Mioglobin
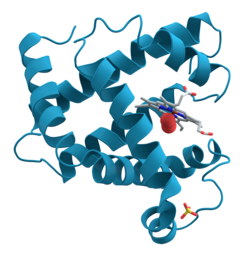
Mioglobin je mišični hemoprotein, sestavljen iz ene polipeptidne verige in ene molekule hema, ki prenaša in hrani kisik v mišicah. Polipeptidna veriga iz 153 aminokislin je organizirana v osem alfa-vijačnic, v katerih je prisotno 78 % vseh aminokislinskih ostankov v proteinu. Molekulska masa proteina je 16.700 daltonov.[1][2]
Za razliko od hemoglobina, s katerim je strukturno soroden,[3] mioglobin ne izraža kooperativnosti pri vezavi kisika. Vezava kisika je tako skorajda neodvisna od parcialnega tlaka kisika v lokalnem tkivu, razen pri izjemno majhnih vrednostih parcialnega tlaka. Nasičenosti mioglobina s kisikom v odvisnosti od parcialnega tlaka kisika zato kaže hiperbolično naravo.
Strukturo mioglobina je s pomočjo rentgenske kristalografije določil John Kendrew s sodelavci leta 1958, za kar je leta 1962 prejel Nobelovo nagrado za kemijo.[4][5]
Barva mesa
urediMioglobin je pigment, odgovoren za rdečo barvo surovega mesa. Barva je delno določena z nabojem železovega iona v mioglobinu ter vezanega kisika. V surovem mesu je železov ion v Fe2+ stanju, na katerega je vezana kisikova molekula. Kuhano meso je rjavkaste barve zaradi Fe3+ stanju, ki je koordiniran z vodno molekulo.
V določenih primeri lahko meso ostane rdečkaste barve kljub kuhanju, npr. pri izpostavitvi nitritom, kjer je na železov ion vezan dušikov oksid (NO), ter izpostavitvi ogljikovem monoksidu (CO), kjer nastane metmioglobin.[6] Rdeča barva je povezana z videzom svežega mesa, zaradi česar je le-to nemalokrat umetno obdelano za doseg takšnega videza za potrebe potrošništva.[7][8]
Medicinski pomen
urediPri razpadu oz. razkroju skeletne mišičnine zaradi poškodbe (rabdomioliza) se sproščajo velike količine mioglobina. Sproščeni mioglobin se filtrira v ledvicah, vendar je toksičen za tubularni epitelij, zaradi česar lahko pride do akutne ledvične odpovedi.[9]
Mioglobin je tudi indikator za potencialno nevarnost miokardičnega infarkta pri pacientih z bolečinami v prsnem košu. Pri tem se za tovrstno diagnozo uporablja kreatin kinaza in troponin v kombinaciji z elektrokardiogramom (EKG).[10]
Opombe in reference
uredi- ↑ Ordway, G.A.; Garry, D.J. (2004). »Myoglobin: an essential hemoprotein in striated muscle«. Journal of Experimental Biology. 207: 3441–3446. doi:10.1242/jeb.01172. PMID 15339940.
- ↑ Nelson, D.L. & Cox, M.M. (2008). Lehninger Principles of Biochemistry, 5. izdaja. NY: W.H. Freeman and Company, str. 155.
- ↑ Lodish H.; Berk A.; Zipursky L.S.; Matsudaira P.; Baltimore D.; Darnell J. (2000). »Evolutionary tree showing the globin protein family members myoglobin and hemoglobin«. Molecular Cell Biology (4. izd.). W. H. Freeman & Co. ISBN 0-7167-3136-3.
- ↑ Kendrew, J.C.; Bodo, G.; Dintzis, H.M.; Parrish, R.G.; Wyckoff, H.; Phillips, D.C. (1958). »A Three-Dimensional Model of the Myoglobin Molecule Obtained by X-Ray Analysis«. Nature. 181 (4610): 662–666. doi:10.1038/181662a0. PMID 13517261.
- ↑ »The Nobel Prize in Chemistry 1962«. Nobelprize.org. Nobelov sklad. Pridobljeno 21. septembra 2021.
- ↑ McGee, H. (2004). On Food and Cooking: The Science and Lore of the Kitchen. NY: Scribner, str. 148. ISBN 0-684-80001-2
- ↑ "Juicy debate: What is fresh meat's true color?" Arhivirano 2007-11-16 na Wayback Machine. Minneapolis Star Tribune, 14. november 2007.
- ↑ "Meat companies defend use of carbon monoxide" Arhivirano 2007-12-03 na Wayback Machine. Minneapolis Star Tribune, 31. oktober 2007.
- ↑ Naka T.; Jones D.; Baldwin I.; Fealy N.; Bates S.; Goehl H.; Morgera S.; Neumayer H.H.; Bellomo R. (2005). »Myoglobin clearance by super high-flux hemofiltration in a case of severe rhabdomyolysis: a case report«. Critical Care. 9: R90–R95. doi:10.1186/cc3034.
- ↑ Weber M.; Rau M.; Madlener K.; Elsaesser A.; Bankovic D.; Mitrovic V.; Hamm C. (2005). »Diagnostic utility of new immunoassays for the cardiac markers cTnI, myoglobin and CK-MB mass«. Clinical Biochemistry. 38: 1027. doi:10.1016/j.clinbiochem.2005.07.011. PMID 16125162.
Glej tudi
urediZunanje povezave
uredi- Kemična sestava in genetski zapis mioglobina (angleško)