Mikrofilament
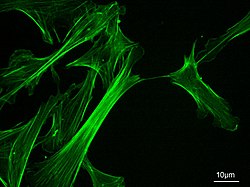
Mikrofilamenti ali aktinski filamenti so beljakovinski nitasti filamenti, ki se nahajajo v citoplazmi evkariontskih celic in gradijo citoskelet. Spadajo med ene izmed treh najbolj pogostih citoskeletnih skupin, pri čemer drugi dve predstavljajo mikrotubuli in intermediarni filamenti. Zgrajeni so iz polimerov molekule aktina, a jih v manjših deležih sestavljajo tudi številne druge beljakovine, z nekaterimi citoplazemskimi in membranskimi proteini pa so v občasni interakciji (denimo miozinom, tropomiozinom in drugimi).[1][2]
Zgodovina
urediMolekularni procesi, v katerih je udeležen aktin, so bili precej dolgo predmet znanstvenih raziskav. Ameriško-nemški botanik George Engelmann je leta 1879 predlagal, da so številna opazovana gibanja znotraj rastlinskih in praživalskih celic (kot so na primer citoplazemski tok, ki ga imenujejo tudi cikloza, in ameboidno premikanje) primitivne različice mišičnega krčenja.
V letu 1930 so Szent-Györgyi in sodelavci prekršili eno izmed glavnih načel biokemije, kjer je bilo v navadi, da se preučuje encime (ki omogočajo sintezo večine celičnih molekul in so zato zelo pogost raziskovalni predmet) in ne strukturnih beljakovin, ki so končni produkt določenih biokemijskih reakcij, ki jih pospešujejo encimi. Zanimanje za gradbene beljakovine je bilo izredno koristno, saj so raziskovalci prišli do mnogih spoznanj, povezanih z mikrofilamenti in ostalimi elementi celičnega citoskeleta.[3]
Značilnosti
urediMikrofilamenti imajo običajno premer od 5 do 7 nanometrov (zaradi česar veljajo za najtanjše predstavnike citoskeletnih elementov)[2] in sestojijo iz dveh sestavljenih niti aktina, ki se zvijeta v dvovijačno (tudi helikalno) obliko.[1][3] Aktinske molekule v tipični živalski celici predstavljajo od 1 do 5% vseh beljakovin, četudi je delež v mišičnih celicah lahko dvakraten. Povprečna koncentracija aktina znotraj posamezne celice je približno 0,5mM.[2]
Posamezne aktinske molekule sestavlja 375 aminokislin, ki oblikujejo več izomorfnih oblik aktina. Po nekaterih podatkih je v živalskih celicah prisotnih 6 izomorfnih oblik, ki se med seboj razlikujejo zgolj na nekaj mestih aminokislinskega zaporedja.[2] Pri sesalcih in pticah se pojavlja šest genov, pri čemer vsak nosi zapis za eno izomorfno obliko aktina. Štiri oblike (α aktin skeletnih mišic, α aktin srčnih mišic, α aktin gladkih mišic in γ aktin gladkih mišic) se običajno izražajo v celicah skeletnih, srčnih in gladkih mišic. Ostali dve izomorfni obliki, β-cito-aktin in γ-cito-aktin se pojavljata v večini evkariontskih celic.[4] Ponekod se uporabljajo nekoliko drugačna poimenovanja za izomorfe aktina, vsem pa je skupno, da so vselej tri oblike alfa (α), dve gama (γ) in ena beta (β).[5]
Aktinu sorodne so beljakovine družine Arp proteinov, pri čemer njihova kratica izhaja iz angleščine (actin related proteins) in jih zato v slovenščini pogosto naslavljamo kar aktinu sorodne beljakovine, sodelujejo pa pri polimerizaciji (tvorbi polimerov iz monomernih enot) mikrofilamentov in prenosu celičnih mešičkov (tudi veziklov) vzdolž mikrotobulov v citoplazmi celice.[2]
Poznamo več morfoloških oblik aktina; glavni sta globularna ali kroglasta (monomerna) oblika G-aktin in nitasta (polimerna) oblika F-aktin, ki jo sestavljajo v verigo nanizani G-aktini. V vsaki aktinski molekuli se nahajajo tudi magnezijevi ioni in molekule ATP ter ADP (ki nastanejo s hidrolizo ATP-ja).[2]
Mikrofilamenti so razmeroma raztegljivi in precej močni. Pri celičnem premikanju se en konec filamenta podaljšuje, medtem ko se drug krči. V literaturi del, kjer se dogaja podaljševanje, imenujejo plus (+) konec, mesto zmanjševanja pa označujejo kot minus (-) konec.[6] Aktinski filamenti zaradi nenehnega krajšanja in podaljševanja veljajo za izjemno dinamične celične strukture. Občasno se več mikrofilamentov poveže s pomočjo različnih pomožnih beljakovin in tvorijo skupke v obliki snopov ali mreže.[2]
Funkcija
urediMed bistvene funkcije aktinskih filamentov spadajo citokineza (tudi delitev citoplazme, ki nastopi po mitozi in zajema končno razdelitev materinske celice na dve hčerinski), ameboidno premikanje (iztezanje delov celice v specifično smer), spreminjanje celične oblike, vpliv na viskoznost citoplazme, endocitoza, eksocitoza, krčenje celice, premikanje z lamelipodiji in filopodiji, in mehanska stabilnost.[7][6] Največja koncentracija mikrofilamentah se v mnogih celicah nahaja tik pod celično membrano (temu območju rečemo skorja ali korteks), zaradi česar lahko citoskeletne strukture po potrebi vplivajo na celično obliko.[6] Aktinski filamenti imajo ključno vlogo tudi pri nekaterih celičnih povezavah, saj se pritrjujejo na beljakovine v celičnih stikih (na primer tesnih in fokalnih).[6]
Ponekod so mikrofilamenti stalne strukture, ki ne spreminjajo svoje zgradbe (denimo znotraj osnovnih krčljivih enot prečno progastih mišic, poimenovanih sarkomer, ki jih gradijo skupaj z beljakovino miozinom).[2]
Proces nastajanja mikrofilamentov
urediZa mikrofilamente je značilna polarnost, kar se odraža že pri njihovih osnovnih gradnikih, aktinskih molekulah, ki imajo na enem koncu vezano molekulo adenozina trifosfata, na drugi strani pa prazno vezavno mesto, kjer bo nastala povezava med dvema aktinoma. Polimerizacija (dodajanje monomernih enot) se odvija pretežno na koncu plus, v manjši meri pa na koncu minus, kjer pa pogosto poteka tudi depolimerizacija (odvzemanje monomernih enot) in posledično krajšanje ali celo razpad mikrofilamentov. Na koncu plus naj bi polimerizacija potekala od 5 do 10 krat hitreje kot na koncu minus.[2] Pri vsaki povezavi dveh aktinskih molekul se odvije hidroliza ATP-ja, ki razpade na fosfat in molekulo ADP, pri čemer slednja ostane vezana na aktinu in zato tako molekulo G-aktina imenujemo kar ADP-aktin. Filament načeloma sestoji iz mnogih ADP-aktinskih molekul G-aktina, medtem ko se ATP-aktinske molekule nahajajo zgolj na plus koncu. Pri polimerizaciji se ves čas dogaja premik monomernih enot iz plus konca proti koncu minus, čemur se v literaturi pripisuje izraz treadmilling.[2][8]
Proces nastajanja aktinskih filamentov delimo v tri faze:
- Nukleacija: molekule G-aktina se zbirajo v kratke in nestabilne oligomere (dolge od 3 do 4 podenote), ki začnejo delovati kot nekakšen agregat, tudi nukleus (ali jedro) in privlačiti nove molekule. Dva monomera se združita v dimer (ki je še nestabilen), ta pa z novim monomerom v trimer, ki lahko že predstavlja nukleus za nukleacijo. Proces občasno traja dalj časa.[2]
- Elongacija (ali podaljševanje): aktinski filamenti pospešeno pridobivajo na svoji dolžini, saj se monomerne enote dodajajo na oba konca. Zaradi tega nastajajo predvsem F-aktini (filamentne oblike).[2]
- Faza ravnotežja: s pojavljanjem F-aktina se prisotnost G-aktina postopoma manjša, dokler oba tipa ne dosežeta približno enake koncentracije. Za to fazo procesa je značilno, da ohranja kritično koncentracijo monomernih enot na vrednosti 0,1 mikrometra. Ob zvišanju poteče polimerizacija G-aktina (podaljša se torej F-aktin), ob znižanju pa depolimerizacija F-aktina (nastane torej več G-aktinskih molekul).[2]
Povezane beljakovine
urediV živalskih celicah, ki niso mišične, se aktinski filamenti tvorijo v bližini celične membrane. Njihova tvorba in delovanje sta odvisna od mnogih drugih beljakovin, med katere spadajo tudi:
- Formini (skupina beljakovin, ki so udeležene pri polimerizaciji aktina, sodelujejo pri citokinezi, celični polarnosti, celični migraciji idr.).[9]
- Arp proteini ali aktinu sorodne beljakovine (na primer Arp2/3 kompleks, ki je pomemben gradnik mikrofilamentov, in Arp 1, ki povezan z beljakovino dineinom sodeluje pri prenosu mešičkov ali celičnih organelov vzdolž mikrotubulov).[10]
- Beljakovine, ki povezujejo aktinske filamente, da nastajajo snopi in se tvorijo tako paralelne kot navzkrižne povezave (denimo α-aktinin, ki povezuje v kontraktilne snope, in fimbrin, ki združuje filamente v tesne snope).[2] V mikrovilih mikrofilamente v snope veže vilin, filamin pa tvori 3D-mrežo aktinskih filamentov.
- Beljakovine, ki povezujejo aktinske monomere (na primer profilin in timozin β4 ).[11]
- Beljakovine, ki s svojo vezavo povzročajo depolimerizacijo mikrofilamentov.[8] Z razgradnjo aktinskih filamentov na manjše delce se zmanjšuje viskoznost citoplazme. Takšne beljakovine so denimo gelsolin, ki vezan na plus konec in v navzočnosti kalcijevih ionov razbija mikrofilamente na manjše fragmente, in kofilin, ki zvišuje raven odcepa (tudi disociacije) monomerov z minus konca.[2]
- Pokrovne beljakovine, ki stabilizirajo mikrofilamente s tem, da se vežejo na njihove konce in ustvarijo zaščitno plast, ki preprečuje depolimerizacijo (denimo tropomodulin, ki se veže na minus konec, in Cap Z, ki se spoji s koncem plus).[8][2]
- Beljakovine, ki mikrofilamente vežejo na celično membrano (na primer spektrin in ankirin, ki tvorita povezave tudi s transmembranskima proteinoma glikoforinom in band 3).[2]
Poleg naštetih so poznane še mnoge druge beljakovine, ki so posredno ali neposredno povezane z mikrofilamenti. Po nekaterih podatkih naj bi jih bilo več kot 100,[2] pričakuje pa se, da bodo odkrite še številne druge.
Sklici
uredi- ↑ 1,0 1,1 Alberts, Bruce; Lewis, Julian; Raff, Martin; Roberts, Keith (2002). Molecular biology of the cell (4. izd.). New York: Garland Science. ISBN 0-8153-3218-1. OCLC 48122761.
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 Jezernik, Kristijan; Sterle, Maksimiljan; Omerzel Vujić, Erika; Lampe Kajtna, Mojca (2012). Celična biologija : učbenik za študente Medicinske fakultete (1. izd.). Ljubljana: DZS. ISBN 978-961-02-0286-8. OCLC 821110606.
- ↑ 3,0 3,1 Wayne, Randy O. (2009). Plant Cell Biology : From Astronomy to Zoology. Burlington: Elsevier Science. ISBN 978-0-08-092127-3. OCLC 761644904.
- ↑ Perrin, Benjamin J; Ervasti, James M (Oktober 2010). »The Actin Gene Family: Function Follows Isoform«. Cytoskeleton (Hoboken, N.j.). Zv. 67, št. 10. str. 630–634. doi:10.1002/cm.20475. ISSN 1949-3584. PMC 2949686. PMID 20737541.
- ↑ Müller, Mirco; Diensthuber, Ralph P.; Chizhov, Igor; Claus, Peter; Heissler, Sarah M.; Preller, Matthias; Taft, Manuel H.; Manstein, Dietmar J. (26. julij 2013). »Distinct Functional Interactions between Actin Isoforms and Nonsarcomeric Myosins«. PLOS ONE (v angleščini). Zv. 8, št. 7. str. e70636. doi:10.1371/journal.pone.0070636. ISSN 1932-6203. PMC 3724804. PMID 23923011.
- ↑ 6,0 6,1 6,2 6,3 Erdani-Kreft, Mateja; Erman, Andreja; Hudoklin, Samo; Resnik, Nataša (2015). Celična biologija (1. izd.). Ljubljana: Medicinska fakulteta, Inštitut za biologijo celice. ISBN 978-961-267-100-6. OCLC 938570032.
- ↑ Gunning, Peter W.; Ghoshdastider, Umesh; Whitaker, Shane; Popp, David; Robinson, Robert C. (1. junij 2015). »The evolution of compositionally and functionally distinct actin filaments«. Journal of Cell Science. Zv. 128, št. 11. str. 2009–2019. doi:10.1242/jcs.165563. ISSN 1477-9137. PMID 25788699.
- ↑ 8,0 8,1 8,2 »Aktin - Wiki FKKT«. wiki.fkkt.uni-lj.si. Pridobljeno 30. novembra 2020.
- ↑ Evangelista, Marie; Zigmond, Sally; Boone, Charles (1. julij 2003). »Formins: signaling effectors for assembly and polarization of actin filaments«. Journal of Cell Science. Zv. 116, št. Pt 13. str. 2603–2611. doi:10.1242/jcs.00611. ISSN 0021-9533. PMID 12775772.
- ↑ Veltman, Douwe M.; Insall, Robert H. (15. avgust 2010). »WASP family proteins: their evolution and its physiological implications«. Molecular Biology of the Cell. Zv. 21, št. 16. str. 2880–2893. doi:10.1091/mbc.E10-04-0372. ISSN 1939-4586. PMC 2921111. PMID 20573979.
- ↑ Xue, Bo; Leyrat, Cedric; Grimes, Jonathan M.; Robinson, Robert C. (28. oktober 2014). »Structural basis of thymosin-β4/profilin exchange leading to actin filament polymerization«. Proceedings of the National Academy of Sciences (v angleščini). Zv. 111, št. 43. str. E4596–E4605. doi:10.1073/pnas.1412271111. ISSN 0027-8424. PMID 25313062. Arhivirano iz prvotnega spletišča dne 1. maja 2021. Pridobljeno 1. maja 2021.