Amonijev železov(II) sulfat
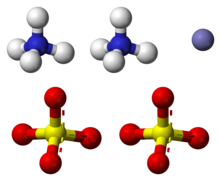
Amonijev železov(II) sulfat ali Mohrova sol je anorganska spojina s formulo (NH4)2Fe(SO4)2•6H2O. Sol vsebuje dva različna kationa, Fe2+ in NH+
4, zato se obravnava kot dvojna sol železovega(II) sulfata in amonijevega sulfata. Spojina je pogost laboratorijski reagent. V vodni raztopini se obnaša podobno kot drugi ferosulfati in tvori vodni kompleks, ki ima oktaedrično molekularno geometrijo.[1]

| |
| |

| |
| Imena | |
|---|---|
| IUPAC ime
amonijev železov(II) sulfat
| |
| Druga imena
fero amonijev sulfat
amonijev železov sulfat Mohrova sol | |
| Identifikatorji | |
3D model (JSmol)
|
|
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.030.125 |
| EC število |
|
PubChem CID
|
|
CompTox Dashboard (EPA)
|
|
| |
| |
| Lastnosti | |
| (NH4)2Fe(SO4)2·6H2O | |
| Molska masa | 284,05 g mol−1 (brezvoden) 392,13 g mol−1 (heksahidrat) |
| Videz | modro zelena trdnina |
| Gostota | 1,86 g/cm3 |
| Tališče | 100 °C (212 °F; 373 K) |
| Vrelišče | ni uporabna |
| Nevarnosti | |
| Glavne nevarnosti | |
| R-stavki (zastarelo) | R36/37/38 |
| S-stavki (zastarelo) | S24/25 |
| NFPA 704 (diamant ognja) | |
| Sorodne snovi | |
| Sorodne snovi | amonijev železov(III) sulfat |
Če ni navedeno drugače, podatki veljajo za material v standardnem stanju pri 25 °C, 100 kPa). | |
| Sklici infopolja | |
Spojina spada v skupino dvojnih sulfatov, znanih tudi kot šeniti ali Tuttonove soli s splošno formulo M2N(SO4)2•6H2O, ki kristalizirajo v monoklinskih kristalih.[2]
Mohrova sol je dobila ime po nemškem kemiku Karlu Friedrichu Mohru (1806–1879), ki je v 19. stoletju uvedel mnogo pomembnih izboljšav v metodologijo titracij.
Uporaba
urediV analizni kemiji se uporablja za titracije, za katere je bolj primeren kot železov(II) sulfat, ker je manj nagnjen k oksidaciji s kisikom iz zraka. Oksidacija Fe2+ v Fe3+ je zelo odvisna od pH in poteka veliko laže pri visokih pH. Amonijevi ioni iz Mohrove soli raztopino rahlo nakisajo in s tem upočasnijo proces oksidacije.[1] Raztopini se v ta namen običajno doda tudi nekaj žveplove kisline.
Amonijev železov(II) sulfat se uporablja v Frickejevih dozimetrih za merjenje velikih doz gama sevanja.[3]
Priprava
urediMohrova sol se pripravlja z raztapljanjem ekvimolarnih količin železovega(II) sulfata heptahidrata (FeSO4•7H2O) in amonijevega sulfata v vodi, rahlo nakisani z žveplovo kislino. Dvojna sol nastane s kristalizacijo iz tako pripravljene raztopine. Kristali soli so modro zelene barve.
Nečistoče
urediStandardna Mohrova sol mora biti najmanj 99 %. Pred uporabo v titraciji se mora rekristalizirati, filtrirati, izprati in posušiti. Med najpogostejšimi nečistočami so Mg, Mn, Ni, Pb in Zn. [4]
Sklici
uredi- ↑ 1,0 1,1 N.N. Greenwood, A. Earnshaw (1997). Chemistry of the Elements. 2. izdaja. Butterworth-Heinemann. ISBN 0080379419.
- ↑ E. Fritz (1926). Inorganic Chemisty. tr P.C.L. Thorne. London: Gurney and Jackson. str. 484–485.
- ↑ C. Hickman, S. Lorrain, J.R. Barthe, G. Portal (1986). Use of Mohr's Salt for High Level Gamma Dosimetry (Up to 108 Gy). Radiatiation Protection Dosimetry (Oxford Journals) 17 (1-4): 255–257.
- ↑ A.I. Vogel (1961). A Text-book of Quantitative Inorganic Analysis Including Elementary Instrumental Analysis. 3. izdaja. Longmans. str. 281–282.
