Tuberkuloza
Tuberkulóza ali jétika (zastarelo tudi sušíca; kratica TBC) je pogosta in mnogokrat smrtna nalezljiva bolezen, ki jo povzročajo različni mikobakterijski sevi, običajno Mycobacterium tuberculosis.[1] Tuberkuloza običajno okuži pljuča, lahko pa tudi druge telesne dele. Širi se po zraku, ko ljudje z aktivno tuberkulozno okužbo kašljajo, kihajo ali kako drugače prenašajo izdihano tekočino skozi zrak.[2] Večinoma so okužbe skrite in brez simptomov. Približno eden od desetih primerov latentne okužbe se sčasoma razvije v aktivno bolezen, ki se za več kot 50 % nezdravljenih oseb konča s smrtjo.
| Tuberkuloza | |
|---|---|
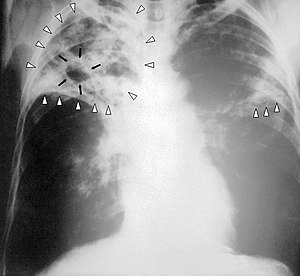 | |
| Rentgenska slika prsnega koša bolnika z napredovano tuberkulozo. Okužba v obeh pljučnih krilih je označena z belimi puščicami, oblikovana votlina s črno puščico. | |
| Specialnost | infektologija, pulmologija |
| Simptomi | kašelj, hemoptiza, hujšanje, vročina, nočno znojenje, bolečina v prsih, utrujenost, mrzlica |
| Pogostost | 0,043—0,045% (Surinam), 0,00033—0,00053% (Islandija), 0,077—0,079% (Ekvador), −0,99—1,01% (Norveška), −0,00088—0,00112% (Francija), 0,0029% (Združene države Amerike), 0,0028% |
| Klasifikacija in zunanji viri | |
| MKB-10 | A15‒A19 |
| MKB-9 | 010‒018 |
| OMIM | 607948 |
| DiseasesDB | 8515 |
| MedlinePlus | 000077 000624 |
| eMedicine | med/2324 emerg/618 radio/411 |
| MeSH | D014376 |
Klasični znaki aktivne okužbe s tuberkulozo so kronični kašelj, krvav izmeček, vročica, nočno potenje in hujšanje (od koder tudi staro ime bolezni – »sušica«). Okužba drugih organov kaže širok spekter simptomov. Diagnoza aktivne tuberkuloze temelji običajno na rentgenskih posnetkih prsnega koša, kot tudi na mikroskopskem pregledu in mikrobiološki kulturi telesnih tekočin. Diagnoza latentne tuberkuloze temelji na tuberkulinskem kožnem testu ali na krvnih preiskavah. Zdravljenje je težavno in zahteva jemanje več antibiotikov v daljšem časovnem obdobju. Socialni stiki se tudi nadzorujejo in po potrebi obravnavajo. Odpornost proti antibiotikom postaja vse večji problem pri okužbah z večkratno odporno tuberkulozo (MDR-TBC). Preprečevanje temelji na presejalnih programih in cepljenju s cepivom na osnovi bacila Calmette‒Guérin (BCG).
Ena tretjina svetovnega prebivalstva naj bi bila okužena z M. tuberculosis,[3] do novih okužb prihaja letno pri približno 1 % prebivalstva.[4] Leta 2007 je ocena števila kroničnih aktivnih primerov po svetu znašala 13,7 milijonov.[5] Leta 2010 so ocenjevali, da se je pojavilo 8,8 milijona novih primerov in 1,5 milijona z boleznijo povezanih smrti, večinoma v državah v razvoju.[6] Število obolelih, gledano absolutno, od leta 2006 dalje pada. Število novih primerov je po letu 2002 upadlo.[6] Porazdelitev tuberkuloze po svetu ni enakomerna, približno 80 % prebivalstva v številnih azijskih in afriških državah je pozitivnega na tuberkulinski test, v ZDA pa je pozitivnih samo 5‒10 % prebivalcev.[1] V razvijajočem se svetu se s tuberkulozo zaradi zmanjšane odpornosti okuži vse več ljudi, predvsem zaradi visoke ravni okužbe s HIV-om in z njo povezanim razvojem AIDS-a.[7]
Znaki in simptomi
urediTuberkuloza lahko okuži katerikoli del telesa, najpogosteje pa se pojavi v pljučih (po tem poznana kot pljučna tuberkuloza).[9] Do ekstrapulmonarne – zunajpljučne – tuberkuloze pride v primeru, ko se tuberkuloza razvije zunaj pljuč, lahko pa zunajpljučna TBC tudi sobiva s pljučno obliko tuberkuloze.[9]
Splošni znaki in simptomi so med drugim vročina, mrzlica, potenje ponoči, izguba teka, hujšanje in utrujenost.[9] Lahko tudi pride do vidnih sprememb na prstih in nohtih.[10]
Pljučna tuberkuloza
urediČe pride do okužbe s tuberkulozo, so običajno prizadeta pljuča (v približno 90 % primerov).[7][11] Simptomi so lahko bolečine v prsih in dolgotrajen kašelj z izpljunkom.[7] Okoli 25 % prizadetih je lahko brez simptomov (asimptomatska okužba).[7] Občasno lahko ljudje izkašljujejo kri v majhnih količinah in, v zelo redkih primerih, lahko okužba razje pljučne arterije, čemur sledi obsežna krvavitev (anevrizma Rasmussena). Tuberkuloza lahko postane kronična in povzroči obsežne brazgotine v zgornjih predelih pljuč. Tuberkuloza pogosteje prizadene zgornje kot spodnje predele pljuč.[9] Razlog za to ni jasen.[1] Lahko da gre za boljši pretok zraka[1] ali pa slabše delovanje limfnega sistema v zgornjem delu pljuč.[9]
Zunajpljučna tuberkuloza
urediV 15‒20 % aktivnih primerov se okužba razširi na organe zunaj pljuč, kar vodi do drugih različic tuberkuloze.[12] Znane so pod skupnim imenom »zunajpljučna tuberkuloza«.[13] Do zunajpljučne tuberkuloze prihaja pogosteje pri ljudeh z okvarjenim imunskim sistemom in pri otrocih. Pri osebah s HIV-om se to pripeti pri več kot 50 % primerov.[13] Do zunajpljučne okužbe pogosto pride na poprsnici (tuberkulozni plevritis), osrednjem živčevju (tuberkulozni meningitis), limfnem sistemu (skrofula vratu), sečilih (urogenitalna tuberkuloza) ter okostju in sklepih (Pottova bolezen hrbtenjače). Če se razširi v kosti, jo imenujejo »kostna tuberkuloza«,[14] ena od oblik osteomielitisa.[1] Včasih tuberkulozni ognojek (absces) predre skozi kožo, kar privede do tuberkuloznega ulkusa.[15] Razjeda, ki izvira bližnjih okuženih bezgavk, je neboleča, širi se počasi in spominja na »podložko za vijak«.[16] Hujša je miliarna tuberkuloza – »razsejana« oblika TBC, ki je zelo razširjena.[9] Miliarna TBC predstavlja približno 10 % zunajpljučnih oblik bolezni.[17]
Vzroki
urediMikobakterije
urediGlavni povzročitelj tuberkuloze je Mycobacterium tuberculosis, aeroben in negibljiv bacil.[9] Visoka vsebnost lipidov je pri tem patogenu odgovorna za številne od njegovih edinstvenih kliničnih značilnosti.[18] Deli se vsakih 16 do 20 ur, kar je zelo počasi v primerjavi z drugimi bakterijami, ki se običajno delijo več kot enkrat na uro.[19] Mikobakterija ima zunanjo membrano v obliki lipidnega dvosloja.[20] Pri barvanju po Gramu se bakterija ali obarva šibko »grampozitivno« ali barvila zaradi visoke vsebnosti lipidov in mikolične kisline v svojo celični steni ne obdrži.[21] MTB preživi v šibkih razkužilih in v obliki endospor preživi tedne dolgo. V naravi lahko bakterija uspeva le v celicah gostiteljicah prizadetega organizma, vendar pa je M. tuberculosis mogoče gojiti v laboratoriju.[22]
S pomočjo histoloških barvil je na izkašljanih vzorcih (izmeček) mogoče MTB dokazati z uporabo svetlobnega mikroskopa. Ker MTB ohranja nekatera barvila tudi po obdelavi s kislo raztopino, je razvrščen kot kislinsko hiter bacil (angl. acid-fast bacillus – AFB).[1][21] Najpogosteje uporabljeni metodi barvanja s hitro kislino sta metoda po Ziehl‒Neelsenu, ki barva bacile AFB svetlo rdeče, da jasno izstopajo na modri podlagi,[23] in pa metoda z avraminom in rodaminom, ki omogoča opazovanje s fluorescenčno mikroskopijo.[24]
Kompleks M. tuberculosis vsebuje še štiri druge mikobakterije, ki povzročajo TBC: M. bovis, M. africanum, M. Canetti in M. microti.[25] M. africanum sicer ni široko razširjena, v nekaterih predelih Afrike pa pomeni pomemben vzrok za TBC.[26][27] Bacil M. bovis je bil nekoč pogost vzrok za tuberkulozo, vendar v razvitih državah z uvedbo pasterizacije mleka v veliki meri ne pomeni več zdravstvenega problema.[1][28] M. canetti se pojavlja redko na območju Afriškega roga. Našli so ga pri izseljencih iz Afrike.[29][30] M. microti je prav tako redek, večinoma se pojavlja pri osebah z imunsko pomanjkljivostjo. Razširjenost tega patogena se je morda doslej precej podcenjevalo.[31]
Druge znane patogene mikobakterije so med drugim Mycobacterium leprae, Mycobacterium avium in Mycobacterium kansasii. Slednji dve vrsti razvrščajo med »netuberkulozne mikobakterije«. Te ne povzročajo ne TBC in ne gobavosti, pač pa pljučna obolenja, ki spominjajo na TBC.[32]
Dejavniki tveganja
urediNa dovzetnost ljudi za okužbe s tuberkulozo vplivajo številni dejavniki. Najpomembnejši dejavnik tveganja na svetovni ravni je HIV. 13 % vseh, ki imajo tuberkulozo, je okuženih s tem virusom.[6] V podsaharski Afriki, kjer je razširjenost okužbe s HIV visoka, je to poseben problem.[33][34] Med ljudmi brez HIV, ki so okuženi s tuberkulozo, jih 5‒10 % v času njihovega življenja aktivno zboleli.[10] Po drugi strani pa med prizadetimi, ki so sočasno okuženi z virusom HIV, 30 % razvije aktivno bolezen.[10]
Tuberkuloza je tesno povezana s prenaseljenostjo in podhranjenostjo. Predstavlja eno glavnih bolezni revščine.[7] Visoko ogroženi so med drugim ljudje, ki si vbrizgavajo nedovoljene droge, prebivalci in zaposleni na območjih, kjer se bolni ljudje zbirajo (npr. zapori in zavetišča za brezdomce), glede zdravstvenih oskrbe in virov revne skupnosti, visoko ogrožene etnične manjšine, otroci v tesnem stiku z visoko ogroženimi bolniki in zdravstveno osebje, ki za te bolnike skrbi.[35]
Kronična pljučna bolezen je še en pomemben dejavnik tveganja. Silikoza povečuje tveganje za približno 30-krat.[36] Kadilci cigaret imajo skoraj dvakrat višje tveganje za TBC kot nekadilci.[37]
Druge zdravstvene okoliščine tudi lahko povečajo tveganje za razvoj tuberkuloze, med drugim alkoholizem[7] in sladkorna bolezen (trikratni porast).[38]
Nekatera zdravila, kot so kortikosteroidi in infliksimab (monoklonsko protitelo anti-TNF α), postajajo čedalje pomembnejši dejavniki tveganja, še posebej v razvitem svetu.[7]
Obstaja tudi genetsko pogojena dovzetnost,[39] njen pomen za zdaj še ni jasen.[7]
Mehanizem
urediPrenos
urediKadar ljudje z aktivno pljučno tuberkulozo kašljajo, kihajo, govorijo, pojejo, ali pljuvajo, oddajajo nalezljive aerosolne kapljice s premerom 0,5–5,0 μm. Pri enkratnem kihu nastane do 40.000 kapljic.[40] Vsaka od teh kapljic lahko prenese bolezen, saj je doza za okužbo s tuberkulozo zelo nizka (že vdih manj kot 10 bakterij lahko povzroči okužbo).[41]
Ljudje z dolgotrajnim, pogostim ali tesnim stikom s tuberkoluznimi osebami so še posebno ogroženi (za stopnjo okužbe se v tem primeru ocenjuje, da znaša 22 %).[42] Oseba z aktivno, vendar nezdravljeno tuberkulozo lahko na leto okuži 10‒15 (ali več) drugih.[3] Do prenosa naj bi prišlo samo pri ljudeh z aktivno tuberkulozo – za latentno okužene se meni, da bolezen ni nalezljiva.[1] Verjetnost prenosa iz ene osebe na drugo je odvisna od številnih dejavnikov, med drugim od števila nalezljivih kapljic, ki jih bolnik širi, od učinkovitosti prezračevanja, trajanja izpostavljenosti, virulence seva M. tuberculosis, ravni imunosti pri neokuženih in od drugih dejavnikov.[43] Širjenje od osebe do osebe je mogoče preprečiti z učinkovito izolacijo oseb z aktivno (»prikrito«) tuberkulozo in z ustreznim režimom zdravil proti TBC. Po približno dveh tednih učinkovitega zdravljenja osebe z aktivno okužbo običajno za druge, kar se nalezljivosti tiče, niso več nevarne.[42] Pri na novo okuženih običajno traja od tri do štiri tedne, da prizadeta oseba postane vir za prenos bolezni na druge.[44]
Patogeneza
urediPri približno 90 % okuženih z M. tuberculosis gre za »latentno okužbo« – skrito okužbo brez znakov,[45] pri čemer doživljenska verjetnost, da se latentna okužba razvije v aktivno bolezen, ne znaša več kot 10 %.[46] Pri osebah s HIV se nevarnost za pojav aktivne TBC poveča na skoraj 10 % na leto.[46] Če se bolezen ne zdravi učinkovito, znaša stopnja smrtnosti pri aktivnih primerih tuberkuloze do 66 %.[3]
Okužba TBC se začne, ko mikobakterije pridejo v pljučne alveole, kjer napadejo alveolarne makrofage in se v njihovih endosomih razmnožujejo.[1][47] Primarno mesto okužbe v pljučih je znano kot »Ghonovo žarišče«. Na splošno se nahaja v zgornjem delu spodnjega režnja ali v spodnjem delu zgornjega režnja.[1] Do pljučne tuberkuloze lahko pride tudi preko obtočil. Ti primeri so znani kot »Simonovo žarišče«, običajno so v vrhu pljuč.[48] Ta prenos preko krvi lahko povzroči širjenje okužbe na bolj oddaljene točke, kot so periferne bezgavke, ledvice, možgani in kosti.[1][49] Bolezen lahko prizadene vse dele telesa, iz neznanih razlogov pa se redko naseli v srce, skeletne mišice, trebušno slinavko ali ščitnico.[50]
Tuberkulozo razvrščajo med granulomatozne vnetne bolezni. Celice, kot so makrofagi, celice ubijalke, limfociti B in fibroblasti, se združujejo v granulome in z limfociti obkolijo okužene makrofage. Granulom preprečuje širjenje mikobakterij in nudi lokalno okolje, v katerem pride do posegov celic imunskega sistema. Bakterije znotraj granuloma lahko zaspijo (postanejo dormantne), kar vodi do latentne okužbe. Druga značilnost granulomov je odmiranje celic (nekroza) v središču tuberklov. S prostim očesom so videti kot mehek, bel sir (kazeozna – sirasta – nekroza).[51]
Če bakterije z območja poškodovanega tkiva zaidejo v krvni obtok, se lahko razširijo po celem telesu in ustvarjajo številna žarišča, ki se vsa kažejo kot majhni, beli tuberkli v tkivu.[52] Ta huda oblika tuberkuloze se imenuje miliarna tuberkuloza in je najbolj pogosta pri majhnih otrocih in pri osebah s HIV.[53] Smrtnost je pri ljudeh s to obliko kljub zdravljenju visoka (približno 30 %).[17][54]
Pri številnih prizadetih prihaja pri bolezni do zagonov in remisij. Uničenje in odmiranje tkiva sta pogosto v ravnovesju s celjenjem in fibrozo.[51] Prizadeto tkivo nadomestijo brazgotine in votline, napolnjene s sirastim nekrotičnem materialom. Med aktivno boleznijo se nekatere od teh votlin lahko povežejo z bronhiji v zračnih kanalih, tako da je snov v njih mogoče izkašljati. Snov vsebuje žive bakterije, čemur sledi širjenje okužbe. Zdravljenje z ustreznimi antibiotiki ubija bakterije in omogoča ozdravljenje. Prizadeta območja, ko so enkrat ozdravljena, nadomesti brazgotinasto tkivo.[51]
Diagnoza
urediAktivna tuberkuloza
urediDiagnosticirati aktivno tuberkulozo samo na podlagi znakov in simptomov je težko,[55] prav tako tudi bolezen pri osebah s suprimiranim imunskim sistemom.[56] Na diagnozo TB pa je treba pomisliti pri pacientih z znaki pljučnega obolenja ali splošnimi simptomi, ki trajajo dlje kot dva tedna.[56] Rentgensko slikanje prsnega koša in multipla kultura izpljunka za acido-bacile sta običajno del začetne ocene.[56] Testi sproščanja interferonov in tuberkulinski kožni testi v državah v razvoju nekoristni.[57][58] IGRA pozna pri osebah s HIV podobne meje.[58][59]
Diagnoza TB je jasna, če se za M. tuberculosis ugotovi prisotnost v kliničnem vzorcu (kot so npr. izmeček, gnoj ali tkivo, dobljeno z biopsijo). Ker gre za počasi rastoč organizem, je postopek kulture težaven in traja pri vzorcih krvi ali izmečka od dva do šest tednov.[60] Z zdravljenjem se zato pogosto prične, še preden kulture diagnozo potrdijo.[61]
S testi amplifikacije DNK in preskusom na adenozin deaminazo je mogoče TB hitro dokazati.[55] Teh testov pa se rutinsko ne priporoča, saj le redko vplivajo na to, kako se primer terapira.[61] Krvni testi za odkrivanje protiteles niso ne specifični ne občutljivi, zato se jih ne priporoča.[62]
Skrita tuberkuloza
urediTest je pogosto uporablja pri pregledih oseb z velikim tveganjem za tuberkulozo.[56] Pri predhodno imuniziranih osebah lahko pride do lažno pozitivnih rezultatov testa.[63] Test je lahko lažno negativen pri osebah, ki imajo sarkoidozo ali Hodgkinov limfom, ki so podhranjene, ali pa (zanimivo) pri posameznikih z dejansko aktivno tuberkulozo.[1] Za osebe s pozitivnim izidom tuberkulinskega testa se priporočajo test krvi na sproščanje gama interferona (Interferon gamma release assay - IGRA).[61] Na te teste imunizacija ali okolijske mikobakterije večinoma ne vplivajo, tako da je napačno pozitivnih izidov pri njih manj.[64] Vplivajo pa nanje M. szulgai, M. marinum in M. kansasii.[19] Testi IGRA lahko povečajo občutljivost, kadar se uporabljajo hkrati s kožnim testom, so pa lahko da manj občutljivi kot kožni test, če se uporabljajo brez njega.[65]
Preventiva
urediPrizadevanja za preprečevanje in nadzor tuberkuloze temeljijo predvsem na cepljenju dojenčkov in na odkrivanju in ustreznem zdravljenju aktivnih primerov.[7] Svetovna zdravstvena organizacija je žela nekaj uspeha s terapevtskimi izboljšavami, ki so povzročile majhen padec v številu obolenj.[7]
Cepiva
urediOd leta 2011 dalje je na voljo le cepivo na osnovi bacila Calmette‒Guérin (BCG), ki je sicer učinkovito proti širjenju bolezni v otroštvu, vendar pred okužbo s pljučno tuberkulozo ne ščiti zanesljivo.[66] Kljub temu je po vsem svetu najbolj pogosto uporabljeno cepivo, s katerim se cepi več kot 90% vseh otrok.[7] Tako pridobljena imunost pa po približno desetih letih začne padati.[7] Kot je tuberkuloza v Kanadi, Veliki Britaniji in Združenih državah Amerike večinoma neobičajna, se z BCG cepi samo visoko ogrožene ljudi.[67][68][69] Eden od razlogov, zakaj naj se cepiva ne rabi, so lažno pozitivni tuberkulinski testi na koži, tako da je za presejalne programe nekoristen.[69] V razvoju so trenutno številna nova cepiva.[7]
Javno zdravje
urediSvetovna zdravstvena organizacija je leta 1993 TB razglasila za "svetovni zdravstveni izziv",[7] leta 2006B pa je Združenje Ustavimo TB (stop TB) razvilo globalni načrt, kako zaustaviti tuberkulozo, z namenom do leta 2015 rešiti 14 milijonov življenj.[70] Cilja za leto 2015 verjetno ne bo mogoče doseči, predvsem zaradi porasta v primerih s HIV povezane tuberkuloze in zaradi pojava tuberkuloze, odporne proti več zdravilom (»multiple drug-resistant«, skrajšano MDR-TB).[7] Sistem, za razvrstitev tuberkuloze, ki ga je razvilo Združenje za prsni koš ZDA, se uporablja predvsem v javnih zdravstvenih programih.[71]
Obvladovanje
urediZa zdravljenje TBC se uporablja antibiotike, ki ubijajo bakterije. Uspešno zdraviti TBC je težko; neobičajna struktura in kemična sestava celičnih sten pri mikobakterijah ovirata vstop zdravilom in tako onemogočata delovanje marsikaterega antibiotika.[72] Najbolj pogosto uporabljena antibiotika sta isoniazid in rifampicin, zdravljenja pa lahko traja tudi več mesecev.[43] Skrito TB se običajno zdravi z enim samim antibiotikom.[73] za aktivna obolenja s TB pa je najboljša kombinacija več antibiotikov, ki zmanjšuje tveganje, da se pri bakterijah razvije odpornost proti antibiotikom.[7] Latentno okužene ljudi se prav tako zdravi, da se pri njih prepreči kasnejši izbruh aktivne TB.[73] WHO priporoča terapijo pod neposrednim nadzorom zdravstvenega osebja, tako da se zagotovi redno jemanje zdravila; cilj je omejiti število bolnikov, ki zdravil ne jemljejo redno.[74] Dokazi, da je ta pristop boljši kot če se zdravila jemljejo nenadzorovano, so šibki.[75] Pristop, s katerim se ljudi opominja, kako pomembno je zdravljenje, pa zgleda učinkuje.[76]
Nov pojav bolezni
urediOb novem pojavu pljučne TB od 2010 dalje priporočajo terapijo, ki traja šest mesecev, s kombinacijo antibiotikov, ki vsebujejo rifampicin, isoniazid, pirazinamid in etambutol prva dva meseca, zadnje štiri pa samo rifampicin in isoniazid.[7] Pri visoki odpornosti proti izoniazidu se lahko zadnje štiri mesece daje alternativno etambutol.[7]
Ponavljajoča obolenja
urediČe se tuberkuloza ponavlja, je pomembno pred začetkom zdravljenja s testi ugotoviti, na katere antibiotike je povzročitelj občutljiv.[7] Če se ugotovi, da gre za TB, ki je multirezistentna, to je odporna na več zdravil (MDR-TB), priporočajo jemati najmanj 4 učinkovite antibiotike 19 do 24 mesecev dolgo.[7]
Odpornost proti zdravilom
urediDo prvotne odpornosti pride, ko se prizadeta oseba okuži z odpornim sevom TB. Pri osebi s popolnoma občutljivo TB se lahko med zdravljenjem zaradi neustreznega zdravljenja razvije sekundarna (pridobljena) upornost , če bolnik zdravil ne jemlje ustrezno predpisani shemi (neskladnost z navodili zdravnika), ali če se uporablja zdravila nizke kakovosti.[77] Proti zdravilom odporna TB je resen zdravstveni problem v številnih državah v razvoju, saj je podaljšuje zdravljenje dlje in zahteva dražja zdravila. MDR-TB se definira kot odpornost proti najbolj uspešnim zdravilom prve izbire pri TB: rifampicin and isoniazid. Tuberkuloza, prekomerno odporna proti zdravilom, je odporna proti trem ali več razredom zdravil druge izbire.[78]
Proti zdravilom popolnoma odporna tuberkuloza je odporna proti vsem zdravilom, ki so trenutno na voljo.[79] Najprej so jo opazili leta 2003 v Italiji, vendar o njej do 2012 niso široko poročali.[79] Bedakvuilin pogojno podpirajo kot sredstvo proti multirezistentni TB.[80]
Prognoza
uredi ni podatkov 10 10‒25 25‒50 50‒75 75‒100 100‒250 | 250‒500 500‒750 750‒1000 1000‒2000 2000‒3000 3000 |
Okužba se razvije v jasno izraženo TB, ko bacili premagajo obrambo imunskega sistema in se začnejo razmnoževati. Pri primarni TB (pri okoli 1–5 % primerov) pride do tega po začetni okužbi.[1] Latentna okužba pa se v večini primerov pojavi brez očitnih znakov.[1] Ti mirujoči bacili izzovejo aktivno tuberkulozo v 5–10 % teh latentnih primerov, pogosto mnogo let po okužbi.[10]
Imunosupresija, na primer zaradi okužbe s HIV, zviša nevarnost za ponoven izbruh bolezni. Pri osebah, ki so okužene tako z M. tuberculosis kot s HIV, se nevarnost za ponoven pojav bolezni poveča na skoraj 10 % na leto.[1] Študije prstnih odtisov DNK pri sevih M. tuberculosis so pokazale, da ponovna okužba k ponavljajoči se TB prispeva bistveno več, kot so predvidevali doslej.[82] - za območja s pogosto TB cenijo delež pri ponovno aktiviranih primerih TB na več kot 50 %.[83] Verjetnost za smrt zaradi tuberkuloze je znašala leta 2008 4 %, kar pomeni zmanjšanje smrtnosti v primerjavi z letom 1995, ko je le-ta znašala 8 %.[7]
Epidemiologija
urediPribližno tretjina svetovnega prebivalstva je bila okužena s M. tuberculosis,[3] do novih okužb prihaja letno pri približno 1 % prebivalstva.[4] Vendar pa večina okužb z M. tuberculosis ne povzroči tuberkuloze,[85] in 90–95 % okužb ostaja brez simptomov.[45] Leta 2012 je bilo po oceni 8,6 milijona kroničnih aktivnih primerov.[86] Leta 2010 so ugotovili 8,8 milijonov novih primerov tuberkuloze in 1,45 milijona smrtnih žrtev, večinoma v državah v razvoju.[6] Med temi 1,45 milijona smrtnih žrtev je bilo približno 350.000 bolnikov s sočasno okužbo z virusom HIV.[87]
Tuberkuloza je drugi najpogostejši vzrok smrti zaradi nalezljivih bolezni (takoj za HIV/AIDS).[9] Število obolelih, gledano absolutno, od leta 2005 dalje pada in število novih primerov se je po 2002 znižalo.[6] Napredek na Kitajskem je še posebno velik, med letoma 1990 in 2010 jim je uspelo smrtnost zaradi TB zmanjšati za približno 80 %.[87] Tuberkuloza je pogostejša v državah v razvoju; približno 80 % prebivalstva v številnih azijskih in afriških državah je pozitivno na tuberkulinski test, v ZDA pa je pozitivnih samo 5–10 % prebivalcev.[1] Upanje, da se bolezen dobi popolnoma pod nadzor, je močno oslabljeno zaradi številnih dejavnikov, kot so težave pri razvoju učinkovitega cepiva, drag in zamuden diagnostični postopek, obvezno večmesečno zdravljenje, porast s HIV povezane tuberkuloze, in pojav proti zdravilom odpornih primerov po 1980.[7]
Leta 2007 je imel po ocenah med vsemi državami največjo incidenco bolezni Svazi, in sicer 1.200 primerov na 100.000 prebivalcev. Indija je imela največjo skupno incidenco, okoli 2,0 milijona novih primerov.[5] V razvitih državah je tuberkuloza manj pogosta, najti jo je predvsem v urbanih območjih. Število primerov na 100.000 prebivalcev po svetu leta 2010: cel svet 178, Slovenija 332, Ameriki 36, Vzhodno Sredozemlje 173, Evropa 63, jugovzhodna Azija 278, in zahodni Pacifik 139.[87] V Kanadi in Avstraliji je tuberkuloza veliko bolj pogosta med staroselci, zlasti v oddaljenih območjih.[89][90] V ZDA je smrtnost pri aboriginih zaradi tuberkuloze petkrat višja,[91] in med javljenimi primeri TB znaša delež rasnih in etničnih manjšin znaša 84 %.[92]
Pogostnost tuberkuloze je odvisna od starosti prebivalstva. V Afriki v prvi vrsti prizadene mladostnike in mlade odrasle.[93] V državah, kjer je število obolenj dramatično upadlo (na primer v ZDA) , pa predstavlja TB predvsem bolezen starejših ljudi in oseb z oslabljenim imunskim sistemom (dejavniki tveganja so navedeni zgoraj).[1][94]
Slovenija
urediPojavnost tuberkuloze v Sloveniji upada. Leta 1996 je bilo v Sloveniji registriranih 28,3 primera na 100.000 prebivalcev, leta 2002 je pojavnost znašala 17,6/100.000 prebivalcev,[95] leta 2009 pa le še 9,3 primera/100.000 prebivalcev, kar nas uvršča med države z zelo nizko stopnjo obolevnosti.[95][96] V Sloveniji pogosteje zbolevajo moški. Umrljivost za to boleznijo je 1,3–4,2 %.[96]
Zgodovina
urediTuberkuloza je bila prisotna pri ljudeh najkasneje od antike dalje.[7] Najzgodnejši nedvoumni dokaz za M. tuberculosis je najti v ostankih bizona, starih približno 17 tisoč let.[97] Zaenkrat pa ni jasno, ali ima tuberkuloza izvor pri govedu, s kasnejšim prenosom na ljudi, ali pa gre za skupnega prednika.[98] Doslej se je verjelo, da je med procesom udomačitve prišlo do prenosa M. tuberkulosis z živali na ljudi, vendar genska primerjava živalskih in človeških sevov bakterije tega ne potrjuje. Goveji in človeški sev bacila imata skupnega prednika, ki je ljudi morda okužil že v neolitiku.[99] Okostja prazgodovinskih ljudi (4000 pred našim štetjem) kažejo znake tuberkulozo in tuberkulozno gnilobo so dokazali v hrbtenjačah egipčanske mumije iz časov 3000‒4000 pred našim štetjem.[100] Phthisis pomeni v grščini sušico, star izraz za pljučno tuberkulozo;[101] Po Hipokratu je okoli 460 pred našim štetjem phthisis bila najbolj razširjena bolezen. Pravi, da se javlja z vročino in izkašljevanjem krvi in da je skoraj vedno usodna.[102] Genetske študije kažejo, da je v Ameriki TB prisotna od leta 100 našega štetja dalje.[103]
Pred industrijsko revolucijo je folklora tuberkulozo pogosto povezovala z vampirji. Ko je v družini kdo umrl zaradi nje, so drugi okuženi člani družine začeli hirati. Ljudje so verjeli, da je za to kriv umrli, ki iz ostalih družinskih članov izsesava življenje.[104]
Čeprav je Dr Richard Morton leta 1689 za pljučno obliko bolezni dokazal patološko ozadje tuberklov,[105][106] TB zaradi raznolikosti njenih simptomov do 1820 ,niso opredelili kot ene same bolezni, ime tuberkuloza pa je prvi leta 1839 uporabil J. L. Schönlein.[107] Med 1838 in 1845 je Dr. John Croghan, lastnik Mamutske jame, dal prenesti številne ljudi s tuberkulozo v jamo, v upanju, da bodo v čistem jamskem zraku stalne temperature ozdraveli; umrli so po enem letu.[108] Hermann Brehmer je leta 1859 odprl prvi TB sanatorij v Sokolowskem, Poljska.[109]
Bacil, ki povzroča tuberkulozo, Mycobacterium tuberculosis, je 24. marca 1882 odkril in opisal Robert Koch. Za to odkritje je leta 1905 prejel Nobelovo nagrado za fiziologijo ali medicino.[110] Koch ni verjel, da bi si goveja in človeška oblika tuberkuloze bili podobni, tako da so okuženo mleko kot vir okužbe prepoznali šele kasneje. Tveganje za prenos iz tega vira je kasneje dramatično zmanjšal izum procesa pasterizacije. Koch je leta 1890 glicerinski izvleček bacilov tuberkuloze razglasil za "sredstvo" proti tuberkulozi in ga poimenoval »tuberkulin«. Čeprav je bil neučinkovit, so izvleček kasneje uspešno prilagodili za presejalni test za presimptomatsko tuberkulozo.[111]
Albert Calmette in Camille Guérin sta 1906 kot prva na osnovi govejega seva tuberkuloze uspela razviti sredstvo za imunizacijo proti tuberkulozi. Imenovali so ga bacillus Calmette Guèrin (BCG). Z BCG prvič cepili ljudi leta 1921 v Franciji,[112] v ZDA, Združenem kraljestvu in Nemčiji pa so ga začeli široko uporabljati po drugi svetovni vojni.[113]
Tuberkuloza je bila vzrok za zelo široko zaskrbljenost javnosti v 19. in v začetku 20. stoletja kot endemična bolezen revnih. Leta 1815 je v Angliji vsak četrti umrl zaradi »sušice«. V Franciji je TB leta 1918 še vedno bila vzrok smrti v enem od šestih primerov. Ko so 1880 ugotovili, da gre za nalezljivo bolezen, so TB v Veliki Britaniji uvrstili na seznam bolezni, ki jih je treba prijaviti. Začeli so s kampanjami,da ljudje nehajo pljuvati na javnih mestih, okužene revne ljudi pa so "vzpodbujali", da gredo v zaporom podobne sanatorije (v zdraviliščih za srednji in višji razred so bolniki dobivali odlično nego in stalno zdravniško pomoč).[109] Ne glede na (domnevne) ugodnosti "svežega zraka" in pomoč v sanatorijih je celo ob najboljših pogojih v njih umrla v petih letih polovica bolnikov (okoli 1916).[109]
V Evropi je obolevnost s tuberkulozo naraščala od 16. stoletja dalje in dosegla svoj vrh v 18. stoletju, ko je bila vzrok za skoraj četrtino vseh smrti.[114] Smrtnost se je nato do leta 1950 zmanjšala za skoraj 90%.[115] Izboljšave v javnem zdravstvu so še pred prihodom streptomicina in drugih antibiotikov znatno zmanjšale okužbe. Bolezen pa je dalje ostala velika grožnja za javno zdravje, tako da so na primer v Veliki Britaniji Svet za raziskave v medicini (Medical Research Council) leta 1913 ustanovili predvsem z namenom, da se razišče tuberkuloza in njeno ozadje.[116]
Leta 1946 je z odkritjem antibiotika streptomicina učinkovito zdravljenje tuberkuloze postalo realnost. Pred uvedbo tega antibiotika je edino zdravilo (z izjemo zdravilišč) bil kirurški poseg, med drugim "pnevmotoraks tehnika", ki je kolabirala okuženo pljučno krilo, da lahko "počiva" in tuberkulozne brazgotine ozdravi.[117]
Zaradi pojava MDR-TB so kirurške posege ponovno uvedli kot eno od možnosti, ki so na voljo za zdravljenje tuberkuloze. Tekoči kirurški posegi vključujejo odstranitev patoloških kavitet (»bullae«) v pljučih, da se zmanjša število bakterij in poveča izpostavljenost preostalih bakterij zdravilom v krvi; zmanjšuje se tako skupna obremenitev z bakterijami in poveča učinkovitost sistemske antibiotične terapije.[118]
Upanje, da se tuberkulozo popolnoma odpravi (gl koze), se je v osemdesetih letih razblinilo s pojavom proti zdravilom odpornih sevov. Na ponoven pojav tuberkuloze, ki je sledil, je Svetovna zdravstvena organizacija leta 1993 odgovorila z razglasitvijo tuberkuloze kot izrednega svetovnega problema za zdravje[119]
Družba in kultura
urediSvetovna zdravstvena organizacija, Fundacija Bill in Melinda Gates ter ameriška vlada subvencionirajo uporabo novega hitrodelujočega diagnostičnega testa v državah z nizkimi in srednjimi dohodki,[120][121][122] s čimer se je znižal strošek enega testa iz 16,86 $ na 9,98 $. Poleg tega je test točen pri osebah, ki so sočasno okužene z virusom HIV. Ugotovi lahko odpornost proti antibiotiku rifampicinu, s čimer se nakaže, da gre za sev bakterije, večkratno odporen proti zdravilom.[120][123] Leta 2011 so imela še vedno številna revnejša območja le dostop do mikroskopkih preiskav izmečka.[124]
Indija je v letu 2010 imela najvišjo skupno število primerov tuberkuloze po svetu, delno zaradi slabe skrbi za bolezen v zasebnem in javnem zdravstvenem sektorju.[125] Programi, kot je na primer revidiran nacionalni program za nadzor tuberkuloze, so pomagali zmanjšati število okužb pri osebah, ki prejemajo javno zdravstveno oskrbo.[126][127]
Raziskave
urediCepivo BCG ima svoje meje in raziskave in razvoj novih cepiv za TB so v teku.[128] Številni možni kandidati so trenutno v fazah I in II kliničnih preskusov.[128] Da bi izboljšali učinkovitost razpoložljivih cepiv, sta na voljo dva pristopa. Pri enem se BCG dodaja cepivo za podenoto, pri drugi strategiji pa se skuša razviti nova in boljša živa cepiva.[128] MVA85A, primer cepiva s podenoto, ki se trenutno preskuša v Južni Afriki, temelji na gensko spremenjenih Vaccinia virusih.[129] Cepiva bodo upajmo igrala pomembno vlogo pri zdravljenju tako latentne kot aktivne bolezni.[130]
Da bi spodbudili nadaljnji razvoj, raziskovalci in politiki uvajajo nove ekonomske modele za razvoj cepiv, med drugim nagrade, davčne spodbude in vnaprej zagotovljen tržni odvzem.[131][132] Pri razvoju sodelujejo številne skupine, med drugim Stop TB Partnership,[133] Južnoafriška iniciativa za cepivo proti tuberkuloz in Aeras Global TB Vaccine Foundation.[134] Podjetje je prejelo več kot 280.000.000 $ (US) od Fundacije Bill in Melinda Gates za razvoj in licenciranje boljšega cepiva proti tuberkulozi, ki naj bi se ga uporabilo v zelo obremenjenih državah.[135][136]
Za tuberkulozo, ki je odporna proti več zdravilom, se raziskuje številna zdravila, med drugim bedaquiline in delamanid.[137] Bedaquiline je konec 2012 FDA odobrila.[138] Kolikšni sta varnost in učinkovitost teh novih učinkovin še nista čisto jasno, saj rezultati temeljijo na relativno majhnih vzorcih.[137][139] Obstoječi podatki pa kažejo, da je pri bolnikih, ki poleg standardnega zdravljenja TB jemljejo bedaquiline, umrljivost petkrat višja kot bolnikih, ki nove droge ne jemljejo.[140] Posledica so bili članki v strokovni literaturi, ki so odpirali vprašanja glede zdravstvene politike, o tem, zakaj je FDA zdravilo odobrila, in o tem, ali so finančne vezi zdravnikov s podjetjem, ki izdeluje bedaquiline, vplivale na njih ravnanje.[139][141]
Druge živali
urediMikobakterije okužijo veliko različnih živali, med drugim ptice,[142] glodavce,[143] in plazilce.[144] Podvrsta Mycobacterium tuberculosis pa je redko prisotna pri divjih živalih.[145] Prizadevanja za izkoreninjenje goveje tuberkuloze, ki ga povzroča Mycobacterium bovis v govedu in čredah jelenov na Novi Zelandiji, so bila relativno uspešna.[146] Prizadevanja v Veliki Britaniji so bila pri tem manj uspešna.[147][148]
Sklici
uredi- ↑ 1,00 1,01 1,02 1,03 1,04 1,05 1,06 1,07 1,08 1,09 1,10 1,11 1,12 1,13 1,14 1,15 1,16 Kumar V; Abbas AK; Fausto N; Mitchell RN (2007). Robbins Basic Pathology (8 izd.). Saunders Elsevier. str. 516–522. ISBN 978-1-4160-2973-1.
- ↑ Konstantinos A (2010). »Testing for tuberculosis«. Australian Prescriber. 33 (1): 12–18.
- ↑ 3,0 3,1 3,2 3,3 »Tuberculosis Fact sheet N-104«. World Health Organization. november 2010. Pridobljeno 26. julija 2011.
{{navedi splet}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ 4,0 4,1 »Tuberculosis«. World Health Organization. 2002.
- ↑ 5,0 5,1 »Epidemiology« (PDF). Global tuberculosis control: epidemiology, strategy, financing. Svetovna zdravstvena organizacija. 2009. str. 6–33. ISBN 978-92-4-156380-2. Pridobljeno 12. novembra 2009.[mrtva povezava]
- ↑ 6,0 6,1 6,2 6,3 6,4 »The sixteenth global report on tuberculosis« (PDF). Svetovna zdravstvena organizacija. 2011.
- ↑ 7,00 7,01 7,02 7,03 7,04 7,05 7,06 7,07 7,08 7,09 7,10 7,11 7,12 7,13 7,14 7,15 7,16 7,17 7,18 7,19 7,20 7,21 7,22 Lawn, SD; Zumla, AI (2. julij 2011). »Tuberculosis«. Lancet. 378 (9785): 57–72. doi:10.1016/S0140-6736(10)62173-3. PMID 21420161.
- ↑ Schiffman G (15. januar 2009). »Tuberculosis Symptoms«. eMedicineHealth.
- ↑ 9,0 9,1 9,2 9,3 9,4 9,5 9,6 9,7 Gerald L., Mandell; John E., Bennett (2010). Dolin Raphael (ur.). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (7 izd.). Philadelphia, PA: Churchill Livingstone/Elsevier. str. Chapter 250. ISBN 978-0-443-06839-3.
- ↑ 10,0 10,1 10,2 10,3 Gibson, Peter G., ur. (2005). Evidence-based respiratory medicine (1. izd.). Oxford: Blackwell. str. 321. ISBN 978-0-7279-1605-1.
- ↑ Behera, D. (2010). Textbook of pulmonary medicine (2. izd.). New Delhi: Jaypee Brothers Medical Pub. str. 457. ISBN 978-81-8448-749-7.
- ↑ Jindal, S.K., ur. (2011). Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. str. 549. ISBN 978-93-5025-073-0.
- ↑ 13,0 13,1 Golden MP; Vikram HR (2005). »Extrapulmonary tuberculosis: an overview«. American Family Physician. 72 (9): 1761–8. PMID 16300038.
- ↑ Kabra, S.K. (2006). Vimlesh Seth (ur.). Essentials of tuberculosis in children (3. izd.). New Delhi: Jaypee Bros. Medical Publishers. str. 249. ISBN 978-81-8061-709-6.
- ↑ Manual of Surgery. Kaplan Publishing. 2008. str. 75. ISBN 9781427797995.
- ↑ Burkitt, H. George (2007). Essential Surgery: Problems, Diagnosis & Management 4th ed. str. 34. ISBN 9780443103452.
- ↑ 17,0 17,1 Ghosh, Amit K.; Thomas M., Habermann (2008). Mayo Clinic internal medicine : concise textbook. Rochester, MN: Mayo Clinic Scientific Press. str. 789. ISBN 978-1-4200-6749-1.
- ↑ Southwick F (10. december 2007). »Chapter 4: Pulmonary Infections«. Infectious Diseases: A Clinical Short Course, 2nd ed. McGraw-Hill Medical Publishing Division. str. 104, 313–314. ISBN 0-07-147722-5.
- ↑ 19,0 19,1 Jindal, S.K., ur. (2011). Textbook of pulmonary and critical care medicine. New Delhi: Jaypee Brothers Medical Publishers. str. 525. ISBN 978-93-5025-073-0.
- ↑ Niederweis M; Danilchanka O; Huff J; Hoffmann C; Engelhardt H (Marec 2010). »Mycobacterial outer membranes: in search of proteins«. Trends in Microbiology. 18 (3): 109–116. doi:10.1016/j.tim.2009.12.005. PMC 2931330. PMID 20060722.
- ↑ 21,0 21,1 Madison B (2001). »Application of stains in clinical microbiology«. Biotechnic & Histochemistry. 76 (3): 119–125. doi:10.1080/714028138. PMID 11475314.
- ↑ Parish T; Stoker N (1999). »Mycobacteria: bugs and bugbears (two steps forward and one step back)«. Molecular Biotechnology. 13 (3): 191–200. doi:10.1385/MB:13:3:191. PMID 10934532.
- ↑ Medical Laboratory Science: Theory and Practice. New Delhi: Tata McGraw-Hill. 2000. str. 473. ISBN 0-07-463223-X.
- ↑ Semba, Richard D.; Bloem, Martin W., ur. (2008). Nutrition and health in developing countries (2. izd.). Totowa, NJ: Humana Press. str. 291. ISBN 978-1-934115-24-4.
- ↑ van Soolingen D; Hoogenboezem, T.; De Haas, P. E. W.; Hermans, P. W. M.; Koedam, M. A.; Teppema, K. S.; Brennan, P. J.; Besra, G. S.; Portaels, F.; in sod. (1997). »A novel pathogenic taxon of the Mycobacterium tuberculosis complex, Canetti: characterization of an exceptional isolate from Africa«. International Journal of Systematic Bacteriology. 47 (4): 1236–45. doi:10.1099/00207713-47-4-1236. PMID 9336935.
- ↑ Niemann S; Rusch-Gerdes, S.; Joloba, M. L.; Whalen, C. C.; Guwatudde, D.; Ellner, J. J.; Eisenach, K.; Fumokong, N.; Johnson, J. L.; in sod. (2002). »Mycobacterium africanum Subtype II Is Associated with Two Distinct Genotypes and Is a Major Cause of Human Tuberculosis in Kampala, Uganda«. Journal of Clinical Microbiology. 40 (9): 3398–405. doi:10.1128/JCM.40.9.3398-3405.2002. PMC 130701. PMID 12202584.
- ↑ Niobe-Eyangoh SN; Kuaban, C.; Sorlin, P.; Cunin, P.; Thonnon, J.; in sod. (2003). »Genetic Biodiversity of Mycobacterium tuberculosis Complex Strains from Patients with Pulmonary Tuberculosis in Cameroon«. Journal of Clinical Microbiology. 41 (6): 2547–53. doi:10.1128/JCM.41.6.2547-2553.2003. PMC 156567. PMID 12791879.
- ↑ Thoen C; Lobue P; de Kantor I (2006). »The importance of Mycobacterium bovis as a zoonosis«. Veterinary Microbiology. 112 (2–4): 339–45. doi:10.1016/j.vetmic.2005.11.047. PMID 16387455.
- ↑ Acton, Q. Ashton (2011). Mycobacterium Infections: New Insights for the Healthcare Professional. ScholarlyEditions. str. 1968. ISBN 978-1-4649-0122-5.
- ↑ Pfyffer, GE; Auckenthaler, R; van Embden, JD; van Soolingen, D (Oktober–december 2008). »Mycobacterium canettii, the smooth variant of M. tuberculosis, isolated from a Swiss patient exposed in Africa«. Emerging Infectious Diseases. 4 (4): 631–4. doi:10.3201/eid0404.980414. PMC 2640258. PMID 9866740.
- ↑ Panteix, G; Gutierrez, MC; Boschiroli, ML; Rouviere, M; Plaidy, A; in sod. (Avgust 2010). »Pulmonary tuberculosis due to Mycobacterium microti: a study of six recent cases in France«. Journal of Medical Microbiology. 59 (Pt 8): 984–9. doi:10.1099/jmm.0.019372-0. PMID 20488936.
- ↑ American Thoracic Society (1997). »Diagnosis and treatment of disease caused by nontuberculous mycobacteria. To uradno izjavo Združenja ZDA za prsni koš je odobril direktorski svet marca 1997. Medical Section of the American Lung Association«. American Journal of Respiratory & Critical Care Medicine. 156 (2 Pt 2): S1-25. doi:10.1164/ajrccm.156.2.atsstatement. PMID 9279284.
- ↑ »Global tuberculosis control ‒ surveillance, planning, financing WHO Report 2006«. Svetovna zdravstvena organizacija. Pridobljeno 13. oktobra 2006.
- ↑ Chaisson, RE; Martinson, NA (13. marec 2008). »Tuberculosis in Africa--combating an HIV-driven crisis«. The New England Journal of Medicine. 358 (11): 1089–92. doi:10.1056/NEJMp0800809. PMID 18337598.
- ↑ Griffith D; Kerr C (1996). »Tuberculosis: disease of the past, disease of the present«. Journal of Perianesthesia Nursing. 11 (4): 240–245. doi:10.1016/S1089-9472(96)80023-2. PMID 8964016.
- ↑ Cohn, David L.; O'Brien, Richard J.; in sod. (ATS/CDC Statement Committee on Latent Tuberculosis Infection) (Junij 2000). »Targeted tuberculin testing and treatment of latent tuberculosis infection. American Thoracic Society«. MMWR. Recommendations and Reports. 49 (RR-6): 1–51. PMID 10881762.
- ↑ van Zyl Smit, RN; Pai, M; Yew, WW; Leung, CC; Zumla, A; Bateman, ED; Dheda, K (Januar 2010). »Global lung health: the colliding epidemics of tuberculosis, tobacco smoking, HIV and COPD«. European Respiratory Journal. 35 (1): 27–33. doi:10.1183/09031936.00072909. PMID 20044459.
Te analize kažejo, da je za kadilce dvakrat bolj verjetno, da se bodo okužili s TB in zboleli za aktivno obliko bolezni (RR ~1,5 za latetno infekcijo s TB (LTBI) in RR ~2,0 za bolezen TB). Za kadilce je tudi dvakrat bolj verjetno, da umrejo zaradi TB (RR za ~ 2,0 za umrljivost TB), vendar je podatke razložiti zaradi heterogenosti v rezultatih različnih študijah težko interpetirati.
- ↑ Restrepo, BI (15. avgust 2007). »Convergence of the tuberculosis and diabetes epidemics: renewal of old acquaintances«. Clinical Infectious Diseases. 45 (4): 436–438. doi:10.1086/519939. PMC 2900315. PMID 17638190.
- ↑ Müller, M; Hoal, EG (Marec 2010). »Current findings, challenges and novel approaches in human genetic susceptibility to tuberculosis«. Tuberculosis. 90 (2): 71–83. doi:10.1016/j.tube.2010.02.002. PMID 20206579.
- ↑ Cole E; Cook C (1998). »Characterization of infectious aerosols in health care facilities: an aid to effective engineering controls and preventive strategies«. Am J Infect Control. 26 (4): 453–64. doi:10.1016/S0196-6553(98)70046-X. PMID 9721404.
- ↑ Nicas M; Nazaroff WW; Hubbard A (2005). »Toward understanding the risk of secondary airborne infection: emission of respirable pathogens«. J Occup Environ Hyg. 2 (3): 143–54. doi:10.1080/15459620590918466. PMID 15764538.
- ↑ 42,0 42,1 Ahmed N; Hasnain S (2011). »Molecular epidemiology of tuberculosis in India: Moving forward with a systems biology approach«. Tuberculosis. 91 (5): 407–3. doi:10.1016/j.tube.2011.03.006. PMID 21514230.
- ↑ 43,0 43,1 »Core Curriculum on Tuberculosis: What the Clinician Should Know« (PDF) (5 izd.). Centers for Disease Control and Prevention (CDC), Division of Tuberculosis Elimination. 2011. str. 24.
- ↑ »Causes of Tuberculosis«. Mayo Clinic. 21. december 2006. Pridobljeno 19. oktobra 2007.
- ↑ 45,0 45,1 Skolnik, Richard (2011). Global health 101 (2. izd.). Burlington, MA: Jones & Bartlett Learning. str. 253. ISBN 978-0-7637-9751-5.
- ↑ 46,0 46,1 Mainous, Arch G. III.; Pomeroy, Claire, ur. (2009). Management of antimicrobials in infectious diseases : impact of antibiotic resistance (2. izd.). Totowa, N.J.: Humana. str. 74. ISBN 978-1-60327-238-4.
- ↑ Houben E; Nguyen L; Pieters J (2006). »Interaction of pathogenic mycobacteria with the host immune system«. Curr Opin Microbiol. 9 (1): 76–85. doi:10.1016/j.mib.2005.12.014. PMID 16406837.
- ↑ Khan (2011). Essence Of Paediatrics. Elsevier India. str. 401. ISBN 978-81-312-2804-3.
- ↑ Herrmann J; Lagrange P (2005). »Dendritic cells and Mycobacterium tuberculosis: which is the Trojan horse?«. Pathol Biol (Paris). 53 (1): 35–40. doi:10.1016/j.patbio.2004.01.004. PMID 15620608.
- ↑ Agarwal R; Malhotra P; Awasthi A; Kakkar N; Gupta D (2005). »Tuberculous dilated cardiomyopathy: an under-recognized entity?«. BMC Infect Dis. 5 (1): 29. doi:10.1186/1471-2334-5-29. PMC 1090580. PMID 15857515.
- ↑ 51,0 51,1 51,2 Grosset J (2003). »Mycobacterium tuberculosis in the Extracellular Compartment: an Underestimated Adversary«. Antimicrob Agents Chemother. 47 (3): 833–6. doi:10.1128/AAC.47.3.833-836.2003. PMC 149338. PMID 12604509.
- ↑ Crowley, Leonard V. (2010). An introduction to human disease : pathology and pathophysiology correlations (8th izd.). Sudbury, Mass.: Jones and Bartlett. str. 374. ISBN 978-0-7637-6591-0.
- ↑ Anthony, Harries (2005). TB/HIV a Clinical Manual (2. izd.). Geneva: World Health Organization. str. 75. ISBN 978-92-4-154634-8.
- ↑ Jacob, JT; Mehta, AK; Leonard, MK (Januar 2009). »Acute forms of tuberculosis in adults«. The American Journal of Medicine. 122 (1): 12–7. doi:10.1016/j.amjmed.2008.09.018. PMID 19114163.
- ↑ 55,0 55,1 Bento, J; Silva, AS; Rodrigues, F; Duarte, R (Januar–februar 2011). »[Diagnostic tools in tuberculosis]«. Acta medica portuguesa. 24 (1): 145–54. PMID 21672452.
- ↑ 56,0 56,1 56,2 56,3 Escalante, P (2. junij 2009). »In the clinic. Tuberculosis«. Annals of internal medicine. 150 (11): ITC61-614, quiz ITV616. PMID 19487708.
- ↑ Metcalfe, JZ; Everett, CK; Steingart, KR; Cattamanchi, A; Huang, L; Hopewell, PC; Pai, M (15. november 2011). »Interferon-? release assays for active pulmonary tuberculosis diagnosis in adults in low- and middle-income countries: systematic review and meta-analysis«. The Journal of infectious diseases. 204 Suppl 4 (suppl_4): S1120-9. doi:10.1093/infdis/jir410. PMC 3192542. PMID 21996694.
- ↑ 58,0 58,1 Sester, M; Sotgiu, G; Lange, C; Giehl, C; Girardi, E; in sod. (Januar 2011). »Interferon-? release assays for the diagnosis of active tuberculosis: a systematic review and meta-analysis«. The European respiratory journal : official journal of the European Society for Clinical Respiratory Physiology. 37 (1): 100–11. doi:10.1183/09031936.00114810. PMID 20847080.
- ↑ Chen, J; Zhang, R; Wang, J; Liu, L; Zheng, Y; Shen, Y; Qi, T; Lu, H (2011). Vermund, Sten H (ur.). »Interferon-gamma release assays for the diagnosis of active tuberculosis in HIV-infected patients: a systematic review and meta-analysis«. PLoS ONE. 6 (11): e26827. doi:10.1371/journal.pone.0026827. PMC 3206065. PMID 22069472.
- ↑ Diseases, Special Programme for Research & Training in Tropical (2006). Diagnostics for tuberculosis : global demand and market potential. Geneva: World Health Organization on behalf of the Special Programme for Research and Training in Tropical Diseases. str. 36. ISBN 978-92-4-156330-7.
- ↑ 61,0 61,1 61,2 National Institute for Health and Clinical Excellence. Clinical guideline 117: Tuberculosis. London, 2011.
- ↑ Steingart, KR; Flores, LL; Dendukuri, N; Schiller, I; Laal, S; Ramsay, A; Hopewell, PC; Pai, M (Avgust 2011). Evans, Carlton (ur.). »Commercial serological tests for the diagnosis of active pulmonary and extrapulmonary tuberculosis: an updated systematic review and meta-analysis«. PLoS medicine. 8 (8): e1001062. doi:10.1371/journal.pmed.1001062. PMC 3153457. PMID 21857806.
- ↑ Rothel J; Andersen P (2005). »Diagnosis of latent Mycobacterium tuberculosis infection: is the demise of the Mantoux test imminent?«. Expert Rev Anti Infect Ther. 3 (6): 981–93. doi:10.1586/14787210.3.6.981. PMID 16307510.
- ↑ Pai M; Zwerling A; Menzies D (2008). »Systematic Review: T-Cell based Assays for the Diagnosis of Latent Tuberculosis Infection: An Update«. Ann. Intern. Med. 149 (3): 1–9. doi:10.7326/0003-4819-149-3-200808050-00241. PMC 2951987. PMID 18593687.
- ↑ Amicosante, M; Ciccozzi, M; Markova, R (april 2010). »Rational use of immunodiagnostic tools for tuberculosis infection: guidelines and cost effectiveness studies«. The new microbiologica. 33 (2): 93–107. PMID 20518271.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ McShane, H (12. oktober 2011). »Tuberculosis vaccines: beyond bacille Calmette-Guerin«. Philosophical transactions of the Royal Society of London. Series B, Biological sciences. 366 (1579): 2782–9. doi:10.1098/rstb.2011.0097. PMC 3146779. PMID 21893541.
- ↑ »Vaccine and Immunizations: TB Vaccine (BCG)«. Centers for Disease Control and Prevention. 2011. Pridobljeno 26. julija 2011.
- ↑ »BCG Vaccine Usage in Canada - Current and Historical«. Public Health Agency of Canada. september 2010. Arhivirano iz prvotnega spletišča dne 30. marca 2012. Pridobljeno 30. decembra 2011.
{{navedi splet}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) Arhivirano 2012-03-30 na Wayback Machine. - ↑ 69,0 69,1 Teo, SS; Shingadia, DV (Junij 2006). »Does BCG have a role in tuberculosis control and prevention in the United Kingdom?«. Archives of Disease in Childhood. 91 (6): 529–31. doi:10.1136/adc.2005.085043. PMC 2082765. PMID 16714729.
- ↑ »The Global Plan to Stop TB«. World Health Organization. 2011. Pridobljeno 13. junija 2011.
- ↑ Warrell, David A.; Cox, Timothy M.; Firth, John D., ur. (2005). »Sections 1 - 10.«. Oxford Textbook of Medicine (4. ed., paperback. izd.). Oxford [u.a.]: Oxford University Press. str. 560. ISBN 978-0-19-857014-1.
- ↑ Brennan PJ; Nikaido H (1995). »The envelope of mycobacteria«. Annu. Rev. Biochem. 64: 29–63. doi:10.1146/annurev.bi.64.070195.000333. PMID 7574484.
- ↑ 73,0 73,1 Menzies, D; Al Jahdali, H; Al Otaibi, B (Marec 2011). »Recent developments in treatment of latent tuberculosis infection«. The Indian journal of medical research. 133 (3): 257–66. PMC 3103149. PMID 21441678.
- ↑ Arch G.; III Mainous (2010). Management of Antimicrobials in Infectious Diseases: Impact of Antibiotic Resistance. Humana Pr. str. 69. ISBN 1-60327-238-0.
- ↑ Volmink J; Garner P (2007). Volmink, Jimmy (ur.). »Directly observed therapy for treating tuberculosis«. Cochrane Database Syst Rev (4): CD003343. doi:10.1002/14651858.CD003343.pub3. PMID 17943789.
- ↑ Liu, Q; Abba, K; Alejandria, MM; Balanag, VM; Berba, RP; Lansang, MA (8. oktober 2008). Liu, Qin (ur.). »Reminder systems and late patient tracers in the diagnosis and management of tuberculosis«. Cochrane database of systematic reviews (Online) (4): CD006594. doi:10.1002/14651858.CD006594.pub2. PMID 18843723.
- ↑ O'Brien R (1994). »Drug-resistant tuberculosis: etiology, management and prevention«. Semin Respir Infect. 9 (2): 104–12. PMID 7973169.
- ↑ Centers for Disease Control and Prevention (2006). »Emergence of Mycobacterium tuberculosis with extensive resistance to second-line drugs worldwide, 2000-2004«. MMWR Morb Mortal Wkly Rep. 55 (11): 301–5. PMID 16557213.
- ↑ 79,0 79,1 Maryn McKenna (12. januar 2012). »Totally Resistant TB: Earliest Cases in Italy«. Wired. Pridobljeno 12. januarja 2012.
- ↑ »Provisional CDC Guidelines for the Use and Safety Monitoring of Bedaquiline Fumarate (Sirturo) for the Treatment of Multidrug-Resistant Tuberculosis«.
- ↑ »WHO Disease and injury country estimates«. World Health Organization. 2004. Pridobljeno 11. novembra 2009.
- ↑ Lambert M; Hasker, Epco; Deun, Armand Van; Roberfroid, Dominique; Boelaert, Marleen; Van Der Stuyft, Patrick (2003). »Recurrence in tuberculosis: relapse or reinfection?«. Lancet Infect Dis. 3 (5): 282–7. doi:10.1016/S1473-3099(03)00607-8. PMID 12726976.
- ↑ Wang, JY; Lee, LN; Lai, HC; Hsu, HL; Liaw, YS; Hsueh, PR; Yang, PC (15. julij 2007). »Prediction of the tuberculosis reinfection proportion from the local incidence«. The Journal of infectious diseases. 196 (2): 281–288. doi:10.1086/518898. PMID 17570116.
- ↑ »The Stop TB Strategy, case reports, treatment outcomes and estimates of TB burden«. Global tuberculosis control: epidemiology, strategy, financing. Svetovna zdravstvena organizacija. 2009. str. 187–300. ISBN 978-92-4-156380-2. Arhivirano iz prvotnega spletišča dne 30. oktobra 2013. Pridobljeno 14. novembra 2009.
- ↑ »Fact Sheets: The Difference Between Latent TB Infection and Active TB Disease«. Centers for Disease Control. 20. junij 2011. Pridobljeno 26. julija 2011.
- ↑ »Global tuberculosis report 2013«. World Health Organization. 2013.
- ↑ 87,0 87,1 87,2 »Global Tuberculosis Control 2011« (PDF). World Health Organization. Pridobljeno 15. aprila 2012.
- ↑ »WHO report 2008: Global tuberculosis control«. Svetovna zdravstvena organizacija. Pridobljeno 13. aprila 2009.
- ↑ FitzGerald, JM; Wang, L; Elwood, RK (8. februar 2000). »Tuberculosis: 13. Control of the disease among aboriginal people in Canada«. CMAJ : Canadian Medical Association journal / journal de l'Association medicale canadienne. 162 (3): 351–5. PMC 1231016. PMID 10693593.
- ↑ Quah, Stella R.; Carrin, Guy; Buse, Kent; Heggenhougen, Kristian (2009). Health Systems Policy, Finance, and Organization. Boston: Academic Press. str. 424. ISBN 0-12-375087-3.
- ↑ Birn, Anne-Emanuelle (2009). Textbook of International Health: Global Health in a Dynamic World. str. 261. ISBN 9780199885213.
- ↑ »CDC Surveillance Slides 2012 - TB«. Centers for Disease Control and Prevention.
- ↑ »Global Tuberculosis Control Report, 2006 - Annex 1 Profiles of high-burden countries« (PDF). Svetovna zdravstvena organizacija. Arhivirano (PDF) iz spletišča dne 16. julija 2006. Pridobljeno 13. oktobra 2006.
- ↑ »2005 Surveillance Slide Set«. Centers for Disease Control and Prevention. 12. september 2006. Pridobljeno 13. oktobra 2006.
- ↑ 95,0 95,1 Regvat J. et al. Tuberkuloza dojke – redka oblika zunajpljučne tuberkuloze – prikaz primera. ZDRAV VESTN 2004; 73: 211–212
- ↑ 96,0 96,1 Škrjanec Pušenjak M. et l. Pljučna tuberkuloza z nenavadno rentgensko sliko. Medicinski razgledi 2012; 51: 501–506.
- ↑ Rothschild BM; Martin LD; Lev G; Bercovier, Helen; Bar-Gal, Gila Kahila; in sod. (Avgust 2001). »Mycobacterium tuberculosis complex DNA from an extinct bison dated 17,000 years before the present«. Clin. Infect. Dis. 33 (3): 305–11. doi:10.1086/321886. PMID 11438894.
- ↑ Pearce-Duvet J (2006). »The origin of human pathogens: evaluating the role of agriculture and domestic animals in the evolution of human disease«. Biol Rev Camb Philos Soc. 81 (3): 369–82. doi:10.1017/S1464793106007020. PMID 16672105.
- ↑ Comas, I; Gagneux, S (Oktober 2009). Manchester, Marianne (ur.). »The past and future of tuberculosis research«. PLoS Pathogens. 5 (10): e1000600. doi:10.1371/journal.ppat.1000600. PMC 2745564. PMID 19855821.
- ↑ Zink A; Sola C; Reischl U; Grabner W; Rastogi N; Wolf H; Nerlich A (2003). »Characterization of Mycobacterium tuberculosis Complex DNAs from Egyptian Mummies by Spoligotyping«. J Clin Microbiol. 41 (1): 359–67. doi:10.1128/JCM.41.1.359-367.2003. PMC 149558. PMID 12517873.
- ↑ The Chambers Dictionary. New Delhi: Allied Chambers India Ltd. 1998. str. 352. ISBN 978-81-86062-25-8.
- ↑ Hippocrates. Aphorisms. Accessed 7 October 2006.
- ↑ Konomi N; Lebwohl E; Mowbray K; Tattersall I; Zhang D (2002). »Detection of Mycobacterial DNA in Andean Mummies«. J Clin Microbiol. 40 (12): 4738–40. doi:10.1128/JCM.40.12.4738-4740.2002. PMC 154635. PMID 12454182.
- ↑ Sledzik, Paul S.; Nicholas, Bellantoni (Junij 1994). »Bioarcheological and biocultural evidence for the New England vampire folk belief« (PDF). American Journal of Physical Anthropology. 94 (2): 269–274. doi:10.1002/ajpa.1330940210. ISSN 0002-9483. PMID 8085617.
- ↑ Leon Charles Albert Calmette v slovarju Who Named It?
- ↑ Trail RR (april 1970). »Richard Morton (1637-1698)«. Med Hist. 14 (2): 166–74. doi:10.1017/S0025727300015350. PMC 1034037. PMID 4914685.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Zur Pathogenie der Impetigines. Auszug aus einer brieflichen Mitteilung an den Herausgeber. [Müller's] Archiv für Anatomie, Physiologie und wissenschaftliche Medicin. 1839, page 82.
- ↑ Kentucky: Mammoth Cave long on history. Arhivirano 2006-08-13 na Wayback Machine. CNN. 27 February 2004. Accessed 8 October 2006.
- ↑ 109,0 109,1 109,2 McCarthy OR (Avgust 2001). »The key to the sanatoria«. J R Soc Med. 94 (8): 413–7. PMC 1281640. PMID 11461990.
- ↑ Nobelov sklad. Nobelova nagrada v fiziologiji in medicini 1905. Accessed 7 October 2006.
- ↑ Waddington K (Januar 2004). »To stamp out "So Terrible a Malady": bovine tuberculosis and tuberculin testing in Britain, 1890-1939«. Med Hist. 48 (1): 29–48. doi:10.1017/S0025727300007043. PMC 546294. PMID 14968644.
- ↑ Bonah C (2005). »The 'experimental stable' of the BCG vaccine: safety, efficacy, proof, and standards, 1921-1933«. Stud Hist Philos Biol Biomed Sci. 36 (4): 696–721. doi:10.1016/j.shpsc.2005.09.003. PMID 16337557.
- ↑ Comstock G (1994). »The International Tuberculosis Campaign: a pioneering venture in mass vaccination and research«. Clin Infect Dis. 19 (3): 528–40. doi:10.1093/clinids/19.3.528. PMID 7811874.
- ↑ Bloom, Barry R., ur. (1994). Tuberculosis : pathogenesis, protection, and control. Washington, D.C.: ASM Press. ISBN 978-1-55581-072-6.
- ↑ Persson, Sheryl (2010). Smallpox, Syphilis and Salvation: Medical Breakthroughs That Changed the World. ReadHowYouWant.com. str. 141. ISBN 978-1-4587-6712-7.
- ↑ Hannaway, Caroline, ur. (2008). Biomedicine in the twentieth century: practices, policies, and politics. Amsterdam: IOS Press. str. 233. ISBN 978-1-58603-832-8.
- ↑ Shields, Thomas (2009). General thoracic surgery (7th izd.). Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. str. 792. ISBN 978-0-7817-7982-1.
- ↑ Lalloo UG; Naidoo R; Ambaram A (Maj 2006). »Recent advances in the medical and surgical treatment of multi-drug resistant tuberculosis«. Curr Opin Pulm Med. 12 (3): 179–85. doi:10.1097/01.mcp.0000219266.27439.52. PMID 16582672. Arhivirano iz prvotnega spletišča dne 10. maja 2013. Pridobljeno 4. januarja 2014.
- ↑ »Frequently asked questions about TB and HIV«. World Health Organization. Arhivirano iz spletišča dne 25. decembra 2004. Pridobljeno 15. aprila 2012.
- ↑ 120,0 120,1 »Public-Private Partnership Announces Immediate 40 Percent Cost Reduction for Rapid TB Test« (pdf). World Health Organization. 8. avgust 2008.
- ↑ Lawn, SD; Nicol, MP (september 2011). »Xpert- MTB/RIF assay: development, evaluation and implementation of a new rapid molecular diagnostic for tuberculosis and rifampicin resistance«. Future microbiology. 6 (9): 1067–82. doi:10.2217/fmb.11.84. PMC 3252681. PMID 21958145.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ »WHO says Cepheid rapid test will transform TB care«. Reuters. 8. december 2010.
- ↑ »The Stop TB Partnership, which operates through a secretariat hosted by the World Health Organization (WHO) in Geneva, Switzerland« (pdf). STOPTB. 5. april 2013.
- ↑ Lienhardt, C; Espinal, M; Pai, M; Maher, D; Raviglione, MC (november 2011). »What research is needed to stop TB? Introducing the TB Research Movement«. PLoS medicine. 8 (11): e1001135. doi:10.1371/journal.pmed.1001135. PMC 3226454. PMID 22140369.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Mishra, G (2013). »Tuberculosis Prescription Practices In Private And Public Sector In India«. NJIRM. 4 (2): 71–78. Arhivirano iz prvotnega spletišča dne 10. maja 2013. Pridobljeno 4. januarja 2014.
- ↑ Bhargava, Anurag; Pinto, Lancelot; Pai, Madhukar (2011). »Mismanagement of tuberculosis in India: Causes, consequences, and the way forward«. Hypothesis. 9 (1): e7. Arhivirano iz prvotnega spletišča dne 12. januarja 2020. Pridobljeno 4. januarja 2014.
- ↑ Amdekar, Y (Julij 2009). »Changes in the management of tuberculosis«. Indian journal of pediatrics. 76 (7): 739–42. doi:10.1007/s12098-009-0164-4. PMID 19693453.
- ↑ 128,0 128,1 128,2 Martín Montañés, C; Gicquel, B (Marec 2011). »New tuberculosis vaccines«. Enfermedades infecciosas y microbiologia clinica. 29 Suppl 1: 57–62. doi:10.1016/S0213-005X(11)70019-2. PMID 21420568.
- ↑ Ibanga H; Brookes R; Hill P; Owiafe P; Fletcher H; Lienhardt C; Hill A; Adegbola R; McShane H (2006). »Early clinical trials with a new tuberculosis vaccine, MVA85A, in tuberculosis-endemic countries: issues in study design«. Lancet Infect Dis. 6 (8): 522–8. doi:10.1016/S1473-3099(06)70552-7. PMID 16870530.
- ↑ Kaufmann SH (2010). »Future vaccination strategies against tuberculosis: Thinking outside the box«. Immunity. 33 (4): 567–77. doi:10.1016/j.immuni.2010.09.015. PMID 21029966.
- ↑ Webber D; Kremer M (2001). »Stimulating Industrial R&D for Neglected Infectious Diseases: Economic Perspectives« (PDF). Bulletin of the World Health Organization. 79 (8): 693–801.
- ↑ Barder O; Kremer M; Williams H (2006). »Advance Market Commitments: A Policy to Stimulate Investment in Vaccines for Neglected Diseases«. The Economists' Voice. 3 (3). doi:10.2202/1553-3832.1144. Arhivirano iz prvotnega spletišča dne 5. novembra 2006. Pridobljeno 4. januarja 2014.
- ↑ Economic Department of Social Affairs (2009). Achieving the global public health agenda : dialogues at the Economic and Social Council. New York: Organizacija združenih narodov. str. 103. ISBN 978-92-1-104596-3.
- ↑ Zuckerman, Jane N.; Jong, Elaine C., ur. (2010). Travelers' vaccines (2 izd.). Shelton, CT: People's Medical Pub. House. str. 319. ISBN 978-1-60795-045-5.
- ↑ Bill and Melinda Gates Foundation Announcement (12. februar 2004). »Gates Foundation Commits $82.9 Million to Develop New Tuberculosis Vaccines«. Arhivirano iz prvotnega spletišča dne 10. oktobra 2009. Pridobljeno 4. januarja 2014. Arhivirano 2009-10-10 na Wayback Machine.
- ↑ Nightingale, Katherine (19. september 2007). »Gates foundation gives US$280 million to fight TB«.
- ↑ 137,0 137,1 Zumla, A; Hafner, R; Lienhardt, C; Hoelscher, M; Nunn, A (1. marec 2012). »Advancing the development of tuberculosis therapy«. Nature reviews. Drug discovery. 11 (3): 171–2. doi:10.1038/nrd3694. PMID 22378254.
- ↑ »J&J Sirturo Wins FDA Approval to Treat Drug-Resistant TB«. Bloombeg. 31. december 2012. Pridobljeno 1. januarja 2013.
- ↑ 139,0 139,1 Avorn, J (april 2013). »Approval of a tuberculosis drug based on a paradoxical surrogate measure«. JAMA. 309 (13): 1349–1350. doi:10.1001/jama/2013.623. PMID 23430122.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ US Food and Drug Administration. »Briefing Package: NDA 204-384: Sirturo« (PDF).
- ↑ Zuckerman, Diana; Jennifer, Yttri (Januar 2013). »Antibiotics: When science and wishful thinking collide«. Health Affairs.
- ↑ Shivaprasad, HL; Palmieri, C (Januar 2012). »Pathology of mycobacteriosis in birds«. The veterinary clinics of North America. Exotic animal practice. 15 (1): 41–55, v–vi. doi:10.1016/j.cvex.2011.11.004. PMID 22244112.
- ↑ Reavill, DR; Schmidt, RE (Januar 2012). »Mycobacterial lesions in fish, amphibians, reptiles, rodents, lagomorphs, and ferrets with reference to animal models«. The veterinary clinics of North America. Exotic animal practice. 15 (1): 25–40, v. doi:10.1016/j.cvex.2011.10.001. PMID 22244111.
- ↑ Mitchell, MA (Januar 2012). »Mycobacterial infections in reptiles«. The veterinary clinics of North America. Exotic animal practice. 15 (1): 101–11, vii. doi:10.1016/j.cvex.2011.10.002. PMID 22244116.
- ↑ Wobeser, Gary A. (2006). Essentials of disease in wild animals (1 izd.). Ames, Iowa [u.a.]: Blackwell Publ. str. 170. ISBN 978-0-8138-0589-4.
- ↑ Ryan, TJ; Livingstone, PG; Ramsey, DS; de Lisle, GW; Nugent, G; Collins, DM; Buddle, BM (25. februar 2006). »Advances in understanding disease epidemiology and implications for control and eradication of tuberculosis in livestock: the experience from New Zealand«. Veterinary microbiology. 112 (2–4): 211–9. doi:10.1016/j.vetmic.2005.11.025. PMID 16330161.
- ↑ White, PC; Böhm, M; Marion, G; Hutchings, MR (september 2008). »Control of bovine tuberculosis in British livestock: there is no 'silver bullet'«. Trends in microbiology. 16 (9): 420–7. doi:10.1016/j.tim.2008.06.005. PMID 18706814.
{{navedi časopis}}: Vzdrževanje CS1: samodejni prevod datuma (povezava) - ↑ Ward, AI; Judge, J; Delahay, RJ (1. januar 2010). »Farm husbandry and badger behaviour: opportunities to manage badger to cattle transmission of Mycobacterium bovis?«. Preventive veterinary medicine. 93 (1): 2–10. doi:10.1016/j.prevetmed.2009.09.014. PMID 19846226.