Cepivo BCG
Cepivo BCG [besežé] (BCG je okrajšava za bacille Calmette-Guérin, Calmette-Guérinov bacil[1]) je cepivo proti tuberkulozi.[2] Je živo cepivo, pripravljeno iz oslabljenega seva Mycobacterium bovis (Calmette-Guérinov bacil), ki je antigensko zelo podoben sevu Mycobacterium tuberculosis, ki povzroča bolezen pri človeku. Cepljenje na Slovenskem ni več obvezno za vse dojenčke.[3] V državah, kjer tuberkuloza ni pogosta, se namreč priporoča le cepljenje novorojencev z visokim tveganjem za okužbo. Na zemljepisnih območjih, kjer je pa tuberkuloza pogosta, pa se priporoča cepljenje novorojencev čim prej po rojstvu z enim odmerkom cepiva. Priporoča se tudi cepljenje odraslih, ki predhodno še niso prejeli cepiva proti tuberkulozi in so pogosto izpostavljeni okužbi.[4]
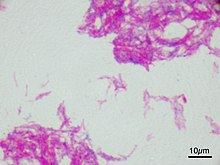 Mikroskopska slika Calmette-Guérinovega bacila, barvanje po Ziehl–Neelsenu, magnification:1,000nn | |
| Klinični podatki | |
|---|---|
| AHFS/Drugs.com | FDA Professional Drug Information |
| Nosečnostna kategorija |
|
| Način uporabe | perkutano |
| Oznaka ATC | |
| Pravni status | |
| Pravni status |
|
Uporaba
urediTuberkuloza
urediCepivo se primarno uporablja za preprečevanje tuberkuloze in se lahko daje novorojencem takoj po rojstvu. Daje se intrakutano (v kožo).[5]
Cepivo je učinkovito v preprečevanju tuberkuloznega meningitisa in diseminirane tuberkuloze pri otrocih. Ne preprečuje pa primarne okužbe pljuč in reaktivacije latentne pljučne okužbe, ki je glavni izvor širjenja bacilov med prebivalstvom. Trajanje zaščite po cepljenju s cepivom BCG novorojencev ni dobro znano, zaščita naj bi padla po 10 do 20 letih.[6]
Podatki iz kliničnih študij o učinkovitosti cepiva so različni in kažejo velike razlike med različnimi zemljepisnimi območji. Raziskave v Veliki Britaniji kažejo na 60- do 80-odstotno učinkovitost, podatki iz nekaterih delov sveta pa kažejo celo na popolno odsotnost zaščitnega učinka. Učinkovitost v državah bliže ekvatorju je po podatkih slabša.[7][8]
Sistematični pregled literature iz leta 1994 navaja, da cepivo BCG zmanjša verjetnost za okužbo za 50 %.[7] Razlike v učinkovitosti v povezavi z različnimi zemljepisnimi območji naj bi bili posledica različnih genetskih in okolijskih dejavnikov, izpostavljenosti drugim povzročiteljem bolezni ter tudi razlik v okoliščinah priprave cepiva (različni bakterijski sevi ter izbor gojišča).[9][10]
Izsledki novejšega sistematičnega pregleda in metaanalize iz leta 2004 kažejo na 19- do 27-odstotno zmanjšanje tveganja za okužbo ter 71-odstotno zmanjšanje tveganja za napredovanje okužbe v aktivno obliko.[11]
Druge mikobakterijske okužbe
uredi- Gobavost – cepivo BCG ščiti tudi proti gobavosti, in sicer je njegova učinkovitost glede na klinične študije 26- do 41-odstotna. Študije s kontrolami primerov in kohortne študije kažejo celo višjo učinkovitost (60 %).[12][13] Vendar pa se cepivo ne uporablja za preprečevanje gobavosti.
- Okužba Mycobacterium ulcerans – podatki kažejo na potencialno zaščito pri okužbi s to mikobakterijo, ki povzroča kožne okužbe v obliki bolezni, imenovane burulska razjeda.[14]
Rak sečnika
urediCepivo BCG se uporablja kot uspešna oblika imunoterapije[15] in predstavlja standardno obliko zdravljenja bolnikov z rakom sečnika že od leta 1977.[15][16] Zdravila na osnovi Calmette-Guérinovega bacila se uporabljajo za zdravljenje površinskega raka sečnika (ki ne vdira v mišico).[15] Dokazi o učinkoviti imunoterapiji z vtočenjem cepiva BCG v sečnik pri takih oblikah raka so na voljo že od poznih 70-ih let prejšnjega stoletja.[17] Mehanizem delovanja ni povsem poznan, kaže pa, da lokalna imunska reakcija pomaga pri boju proti tumorju. Imunoterapija z aplikacijo cepiva BCG v sečnik prepreči ponovitev površinskega raka sečnika v do 67 %.
Neželeni učinki
urediTeden dni po cepljenju se na mestu vnosa (praviloma v koži na nadlahti) pojavi rdeča bunčica (papula), ki se nato nekaj tednov veča in lahko zraste tudi do 2 cm v premer. Njen vrh se lušči in lahko nastane razjeda, ki se v nekaj tednih pozdravi, tvori pa se brazgotina. Slednja je znak učinkovitega cepljenja.[3]
Cepivo je treba aplicirati v kožo (intradermalno). Pri aplikaciji pod kožo (subkutano) lahko pride do lokalno zamejene okužbe, ki se lahko razširi v področne bezgavke in povzroči njihovo vnetje. Če je vnetje bezgavke gnojno, je lahko potrebna aspiracija z iglo, in če še vedno ne pride do ozdravitve, je lahko potrebna kirurška odstranitev z izrezanjem.[18] Pri subkutanem vnosu cepiva lahko pride tudi do dolgotrajne ali globoke razjede, ognojka, granuloma ali hipertrofične brazgotine.[3]
Redko lahko pride do tvorbe ognojka v prsnem ali zadnjičnem predelu zaradi razsoja po krvi ali mezgi.[19] Zelo redka zapleta sta osteomielitis in meningitis.[3] Pri hudih sistemskih zapletih se lahko uporabi zdravljenje s protituberkuloznimi zdravili.[19]
Cepivo ni primerno za bolnike s pomanjkljivim imunskim sistemom, saj lahko pri njih povzroči razsejano (diseminirano) ali življenjsko ogrožajočo okužbo.[20] Od leta 2007 Svetovna zdravstvena organizacija zato več ne priporoča cepljenje otrok, okuženih s HIV-om, četudi je njihovo tveganje za okužbo s tuberkulozo visoko.[21] V tej skupini otrok je sicer tveganje za pojav razsejane okužbe okoli 400 na 100.000.[22][23]
Zgodovina
urediZgodovina razvoja cepiva proti tuberkulozi je močno povezana s cepivom proti črnim kozam. Leta 1854 je Jean Antoine Villemin prvi poročal o goveji tuberkulozi in njenem prenosu na človeka, Robert Koch pa je prvi razločil povzročitelja goveje tuberkuloze (Mycobacterium bovis) in povzročitelja tuberkuloze pri ljudeh (Mycobacterium tuberculosis). Glede na uspehe cepljenja proti črnim kozam s cepivom, ki so ga že v 18. stoletju razvili iz sorodnega virusa, ki je povzročal kravje osepnice, so predpostavljali, da bi lahko s pomočjo seva M. bovis pripravili učinkovito cepivo proti človeški tuberkulozi. Ob koncu 19. stoletja so v Italiji izvedli klinične preskuse z bakterijo M. bovis, vendar so bili rezultati strašljivi, saj se je izkazalo, da je M. bovis enako virulenten kot M. tuberculosis.
Francoski zdravnik in bakteriolog Albert Calmette ter njegov asistent in kasnejši kolega, veterinar Camille Guérin, zaposlena na Pasteurjevem inštitutu v francoskem Lillu, sta v letu 1908 preučevala različne virulentne seve bacila tuberkuloze v različnih gojiščih. Ugotovila sta, da v posebnem gojišču iz glicina, žolča in krompirja uspevajo bacili z manjšo virulentnostjo in preusmerila svoj cilj raziskav v iskanje sevov, ki bi bili dovolj oslabljeni, da bi bili primerni za cepivo. Sev BCG sta izolirala iz glicinsko-krompirjevega gojišča po 239-kratni subkultivaciji virulentnega seva. Z raziskavami sta nadaljevala v prvi svetovni vojni in leta 1919 pridobila avirulentni sev, ki ni bil več sposoben povzročiti bolezni pri poskusnih živalih. Leta 1919 sta se premestila na Pasteurjev inštitut v Parizu.[24] Cepivo BCG so prvikrat nato uporabili pri človeku leta 1921.[6]
Sprejemanje cepiva v javnosti je bilo počasno in hud zaplet s cepljenjem leta 1930 je močno otežil odobravanje javnosti. Poleti 1930 so namreč v nemškem Lübecku cepili 240 novorojencev v prvih desetih dneh po njihovem rojstvu. Pri domala vseh je prišlo do tuberkuloze in 72 jih je umrlo. Kasneje so ugotovili, da je bilo cepivo onesnaženo z virulentnim sevom, ki so ga hranili v istem inkubatorju z nevirulentnim sevom za pripravo cepiva. Zaradi tega dogodka so sledile pravne sankcije proti proizvajalcu.[25] V široko uporabo je cepivo prišlo šele po drugi svetovni vojni.
Sklici
uredi- ↑ http://www.termania.net/slovarji/slovenski-medicinski-slovar/5507821/bcg?query=BCG&SearchIn=All, Slovenski medicinski e-slovar, vpogled: 31. 5. 2016.
- ↑ http://www.termania.net/slovarji/slovenski-medicinski-slovar/5509526/cepivo?query=cepivo&SearchIn=All, Slovenski medicinski e-slovar, vpogled: 31. 5. 2016.
- ↑ 3,0 3,1 3,2 3,3 Zakotnik B., Čižman M., Strle F., Tomažič J. Preprečevanje nalezljivih bolezni. V: Tomažič J., Strle F s sod. Infekcijske bolezni. Ljubljana 2014/2015, str. 224–228.
- ↑ »BCG Vaccine: WHO position paper« (PDF). Weekly epidemiological record. 4 (79): 25–40. 23. januar 2014.
- ↑ »BCG Vaccine | TB Symptoms | Tuberculin Skin Test | PPD | TB Signs«. TB Symptoms. 18. januar 2013. Arhivirano iz prvotnega spletišča dne 29. oktobra 2013. Pridobljeno 2. februarja 2014.
- ↑ 6,0 6,1 Milan Č. Cepljenje v letu 2005. Zdravniški vestnik, 2005, letnik 74, številka 5: 281–284.
- ↑ 7,0 7,1 Colditz, Graham A.; Brewer, TF; Berkey, CS; Wilson, ME; Burdick, E; Fineberg, HV; Mosteller, F (1994). »Efficacy of BCG Vaccine in the Prevention of Tuberculosis«. JAMA. 271 (9): 698–702. doi:10.1001/jama.1994.03510330076038. PMID 8309034.
- ↑ Fine PEM (1995). »Variation in protection by BCG: implications of and for heterologous immunity«. Lancet. 346 (8986): 1339–45. doi:10.1016/S0140-6736(95)92348-9. PMID 7475776.
- ↑ Venkataswamy, Manjunatha M.; Goldberg, Michael F.; Baena, Andres; Chan, John; Jacobs, William R., Jr.; Porcelli, Steven A. (1. februar 2012). »In vitro culture medium influences the vaccine efficacy of Mycobacterium bovis BCG«. Vaccine. 30 (6): 1038–1049. doi:10.1016/j.vaccine.2011.12.044. PMC 3269512. PMID 22189700.
{{navedi časopis}}:|access-date=potrebuje|url=(pomoč) - ↑ FINE, P (1. november 1995). »Variation in protection by BCG: implications of and for heterologous immunity«. The Lancet. 346 (8986): 1339–1345. doi:10.1016/S0140-6736(95)92348-9. PMID 7475776.
- ↑ Roy A, Eisenhut M, Harris RJ, in sod. (2014). »Effect of BCG vaccination against Mycobacterium tuberculosis infection in children: systematic review and meta-analysis«. BMJ. 349: g4643. doi:10.1136/bmj.g4643. PMC 4122754. PMID 25097193.
- ↑ Setia MS, Steinmaus C, Ho CS, Rutherford GW (2006). »The role of BCG in prevention of leprosy: a meta-analysis«. Lancet Infect Dis. 6 (3): 162–70. doi:10.1016/S1473-3099(06)70412-1. PMID 16500597.
- ↑ Merle, Corinne SC; Cunha, Sergio S; Rodrigues, Laura C (2010). »BCG vaccination and leprosy protection: Review of current evidence and status of BCG in leprosy control«. Expert Review of Vaccines. 9 (2): 209–22. doi:10.1586/ERV.09.161. PMID 20109030.
- ↑ Tanghe, A.; J. Content; J. P. Van Vooren; F. Portaels; K. Huygen (2001). »Protective efficacy of a DNA vaccine encoding antigen 85A from Mycobacterium bovis BCG against Buruli ulcer«. Infection and Immunity. 69 (9): 5403–5411. doi:10.1128/IAI.69.9.5403-5411.2001. PMC 98650. PMID 11500410.
- ↑ 15,0 15,1 15,2 Rentsch, Cyrill A.; Birkhäuser, Frédéric D.; Biot, Claire; Gsponer, Joël R.; Bisiaux, Aurélie; Wetterauer, Christian; Lagranderie, Micheline; Marchal, Gilles; Orgeur, Mickael; Bouchier, Christiane; Bachmann, Alexander; Ingersoll, Molly A.; Brosch, Roland; Albert, Matthew L.; Thalmann, George N. (1. oktober 2014). »Bacillus Calmette-Guérin Strain Differences Have an Impact on Clinical Outcome in Bladder Cancer Immunotherapy«. European Urology. 66 (4): 677–688. doi:10.1016/j.eururo.2014.02.061.
{{navedi časopis}}:|access-date=potrebuje|url=(pomoč) - ↑ Brandau, S.; Suttmann, H. (2007). »Thirty years of BCG immunotherapy for non-muscle invasive bladder cancer: a success story with room for improvement«. Biomed Pharmacother. 61: 299–305. doi:10.1016/j.biopha.2007.05.004.
{{navedi časopis}}:|access-date=potrebuje|url=(pomoč) - ↑ Lamm DL, Blumenstein BA, Crawford ED (1991). »A randomized trial of intravesical doxorubicin and immunotherapy with bacille Calmette-Guerin for transitional-cell carcinoma of the bladder«. N Engl J Med. 325 (2): 1205–9. doi:10.1056/NEJM199110243251703. PMID 1922207.
- ↑ Cuello-García, Carlos A.; Pérez-Gaxiola, Giordano; Jiménez Gutiérrez, Carlos (1. januar 2013). »Treating BCG-induced disease in children«. The Cochrane Database of Systematic Reviews. 1: CD008300. doi:10.1002/14651858.CD008300.pub2. ISSN 1469-493X. PMID 23440826.
- ↑ 19,0 19,1 Govindarajan KK, Chai FY (2011). »BCG adenitis — need for increased awareness«. Mal J Med Sci. 18 (2): 67–70. Malaysian Journal of Medical Sciences Arhivirano 2012-03-26 na Wayback Machine.
- ↑ Centers for Disease Control and Prevention (1996). »The role of BCG vaccine in the prevention and control of tuberculosis in the United States: a joint statement of the Advisory Council for the Elimination of Tuberculosis and the Advisory Committee on Immunization Practices«. MMWR Recomm Rep. 45 (RR-4): 1–18. PMID 8602127.
- ↑ WHO (2007). »Revised BCG vaccination guidelines for infants at risk for HIV infection«. Wkly Epidemiol Rec. 82 (21): 193–6. PMID 17526121.
- ↑ Trunz BB, Fine P, Dye C (2006). »Effect of BCG vaccination on childhood tuberculous meningitis and miliary tuberculosis worldwide: a meta-analysis and assessment of cost-effectiveness«. Lancet. 367 (9517): 1173–80. doi:10.1016/S0140-6736(06)68507-3. PMID 16616560.
- ↑ Mak TK, Hesseling AC, Hussey GD, Cotton MF (2008). »Making BCG vaccination programs safer in the HIV era«. Lancet. 372 (9641): 786–7. doi:10.1016/S0140-6736(08)61318-5. PMID 18774406.
- ↑ Fine PE, Carneiro IA, Milstein JB, Clements CJ (1999). Issues relating to the use of BCG in immunization programs. Geneva: WHO.
- ↑ Rosenthal SR. (1957). BCG vaccination against tuberculosis. Boston: Little, Brown & Co.