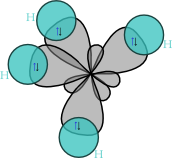
Hibridizacija orbital
Hibridizácija je v kemiji linearna kombinacija atomskih orbital približno enake energije, pri čemer se tvorijo hibridne ali hibridizirane orbitale. Hibridne oribtale so enakega energijskega nivoja in imajo posebno geometrično razvrstitev.
Teorija hibridizacije je posledica nezmožnosti njenih predhodnih teorij razlage molekul, kot je denimo metan (CH4).
Elektronska konfiguracija ogljika je 1s² 2s² 2px¹ 2py¹, oziroma, če to narišemo:
Teorija valenčnih vezi bi predvidela, glede na dve napol napolnjeni orbitali (2px in 2py), da C tvori dve kovalentni vezi. CH2 pa sploh ne obstaja, in ta teorija ne more predvideti eksperimentalno dokazanega obstoja molekule CH4.
Med tvorbo vezi se sprošča energija, ki omogoča enemu elektronu iz 2s prehod v orbitalo 2pz (vzbujeno stanje), kar privede do sledeče elektronske razvrstitve:
Običajno orbitale 2s in 2p nimajo enake energije, vendar pa so poskusi pokazali, da so vse vezi v CH4 enake, in imajo tedaj enako energijo. Govorimo lahko o hibridnih atomskih orbitalah sp³. Hibridizacija je tipa sp³, ker je energijski nivo s¹ + p¹ + p¹ + p¹; seštevek zgornjih števil da vrednost sp³ (beri: »es pe tri«).
V CH4 se štiri hibridne orbitale sp³ frontalno prekrivajo z vodikovimi orbitalami s, kar so štiri vezi sigma (σ). Oblika je tetraedrična.
Podobno se lahko razloži druge molekule, na primer eten (C2H4). Dva ogljikova atoma sta hibridizirana (sp²); orbitala 2pz¹ ni hibridna. Hibridni orbitali vsakega ogljikovega atoma se frontalno prekrivata z orbitalami s vodika, ena hibridna orbitala se frontalno prekriva s hibridno orbitalo drugega C-atoma (skupaj imamo torej pet vezi sigma), orbitali 2pz pa se prekrivata stransko in tvorita vez pi (π). Oblika vsakega dela molekule je trikotna ravninska.
Molekulska oblika
urediHibridizacija pomaga pri razlagi oblike molekul.
- AX2 (npr. BeCl2): hibridizacija sp; linearna oblika
- AX3 (npr. BCl3): hibridizacija sp²; trikotna ravninska oblika
- AX4 (npr. CCl4): hibridizacija sp³; tetraedrična oblika
- AX5 (npr. PCl5): hibridizacija sp³d; trikotna bipiramidalna oblika
- AX6 (npr. SF6): hibridizacija sp³d²; oktaedrična (oziroma kvadratna bipiramidalna) oblika
- AX7 (npr. IF7): hibridizacija sp³d³; pentagonalno bipiramidalna oblika
Ta princip deluje, če na centralnem atomu ni neveznih elektronskih parov. Če so, morajo biti všteti v število Xi. Na primer, v vodi (H2O) ima kisikov atom dve vezi z vodikom in dva nevezna elektronska para (kar lahko ugotovimo tudi s teorijo valenčnih vezi prek elektronske konfiguracije), kar pomeni, da so štirje 'elementi' na kisiku. Model molekule je potemtakem AX4: poteče hibridizacija sp³, razporeditev elektronov v H2O je tetraedrična. Oblika molekule pa je upognjena, saj prosti elektronski pari niso vidni, poleg tega pa je treba misliti tudi na repulzije med elektronskimi pari. Kot HOH je okrog 104.5 stopinj.