Blok f
Blok f periodnega sistema elementov je sestavljen iz elementov, katerih atomi imajo v osnovnem stanju elektrone z najvišjo energijo na orbitali f. Elementi se imenujejo tudi notranji prehodni elementi ali redke zemeljske kovine.
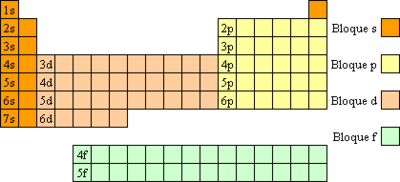
V nasprotju z drugimi bloki periodnega sistema so elementi v bloku f razvrščeni po periodi oziroma po naraščajočih vrstnih številih in ne po skupinah s podobnimi elektronskimi konfiguracijami. Blok f je zato razdeljen v dve skupini: lantanoidi in aktinoidi.[1][2]
Elementi iz bloka f so, tako kot elementi iz bloka s, zelo reaktivne kovine. Na zraku se zelo lahko vnamejo, z vodo pa tvorijo hidrokside in vodik. Imajo večje gostote ter višja tališča in vrelišča od alkalijskih zemeljskih kovin. Zaradi velike reaktivnosti je njihova uporabnost omejena. Pridobivajo se z elektrolizo talin njihovih kloridov, ker elektrolize raztopin zaradi velike reaktivnosti ne pridejo v poštev.
Večina spojin elementov iz bloka f so ionske soli z M3+ ioni, ki so v vodnih aztopinah pogosto hidratizirane. Cerij tvori tudi nekaj spojin, v katerih je v oksidacijskem stanju 4+, na primer CeO2, ki so močni oksidanti. Aktinoidi od protaktinija do americija lahko s svojimi f elektroni sodelujejo v tvorbi kemijskih vezi in tvorijo spojine, v katerih imajo oksidacijska stanja od 2+ do 6+. Težji aktinoidi od kirija do lavrencija pritegnejo notranje f elektrone proti jedru, tako da ne morejo sodelovati pri tvorbi vezi. V spojinah zato nastopajo samo kot M 3+ ioni.
Reference uredi
Glej tudi uredi
Zunanje povezave uredi
- Slike f-orbital Arhivirano 2012-03-21 na Wayback Machine.